题目内容
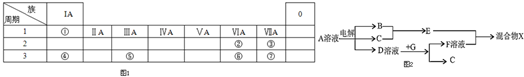
18.短周期元素X、Y、Z、W在元素周期表中的位置如表所示,其中X所处的周期序数与主族序数之和为8.下列说法错误的是( )| X | Y | ||
| Z | W |
| A. | W的原子半径最大 | |
| B. | Z与X形成的化合物难溶于水 | |
| C. | Y的单质不能与水反应 | |
| D. | Z元素的氧化物对应水化物的酸性一定弱于W的氧化物对应水化物的酸性 |
分析 短周期元素X、Y、Z、W,根据元素在周期表中的位置知,X和Y位于第二周期,Z和W位于第三周期,X所处的周期序数与主族序数之和为8,则X位于第VIA族,所以X是O元素,则Y是F元素、Z是Si元素、W是S元素,
A.电子层数越多,其原子半径越大,电子层结构相同,其原子半径随着原子序数的增大而减小;
B.Z与X形成的化合物为二氧化硅;
C.Y为F元素,氟气与水反应生成氧气和氟化氢;
D.硅酸的酸性小于硫酸或亚硫酸.
解答 解:短周期元素X、Y、Z、W,根据元素在周期表中的位置知,X和Y位于第二周期,Z和W位于第三周期,X所处的周期序数与主族序数之和为8,则X位于第VIA族,所以X是O元素,则Y是F元素、Z是Si元素、W是S元素,
A.电子层数越多,其原子半径越大,电子层结构相同,其原子半径随着原子序数的增大而减小,则Z的半径最大,故A错误;
B.Z与X形成的化合物为二氧化硅,二氧化硅难溶于水,故B正确;
C.Y为F元素,氟气与水反应生成氧气和氟化氢,故C错误;
D.硅酸难溶于水,酸性很弱,硅酸的酸性小于硫酸或亚硫酸,故D正确;
故选AC.
点评 本题考查了元素位置、结构和性质的关系及应用,根据元素在周期表中的位置推断元素,明确元素周期律是解本题关键,题目难度不大.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
8.下列反应中不属于加成反应的是( )
| A. | 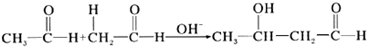 | |
| B. | CH2=CH-CH=CH2+2H2$→_{△}^{催化剂}$CH3-CH2-CH-CH3 | |
| C. | 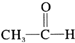 +H2$→_{△}^{催化剂}$CH3-CH-OH +H2$→_{△}^{催化剂}$CH3-CH-OH | |
| D. | CH3-CH2Br+NaOH$→_{△}^{H_{2}O}$CH3-CH2OH+NaBr |
6.磁流体是电子材料的新秀,它既具有固体的磁性,又具有液体的流动性.制备时将FeSO4和Fe2(SO4)3的溶液等物质的量混合,滴入稍过量的氢氧化钠溶液,随后加入油酸钠溶液,即可生成黑色、分散质粒子直径在5.5nm~36nm的磁流体.下列说法正确的是( )
| A. | 所得的分散系属于胶体,可发生丁达尔效应 | |
| B. | 所得的分散系中,分散质的主要成分为FeO | |
| C. | 该分散系进行电泳实验时,阳极周围黑色加深 | |
| D. | 往油酸钠水溶液中滴加浓溴水振荡,无明显现象 |
3.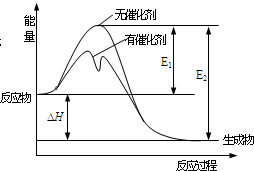 2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
 2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )| A. | 该反应为吸热反应 | |
| B. | 升高温度,不影响活化分子百分数 | |
| C. | 使用催化剂使该反应的反应热发生改变 | |
| D. | E1-E2=△H |
7.某药物中间体X的结构如图所示,下列说法正确的是( )
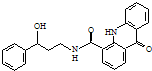

| A. | 该X的分子式为C23H25N2O3 | |
| B. | 每个X分子中含有2个手性碳原子 | |
| C. | 1 mol X最多能与9 mol H2发生加成反应 | |
| D. | X能发生水解、氧化和消去反应 |
16.下列说法正确的是( )
| A. | 单位物质的量的气体所占的体积就是气体摩尔体积 | |
| B. | 摩尔是物质的量的单位 | |
| C. | 阿伏加德罗常数就是6.02×1023 | |
| D. | CO2的摩尔质量为44g |

 $\stackrel{KMnO_{4}/H+}{→}$RCOOH+
$\stackrel{KMnO_{4}/H+}{→}$RCOOH+
 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +H2O
+H2O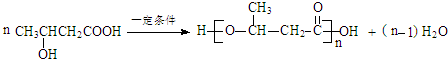 .
. .
.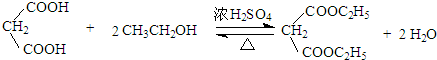 .
.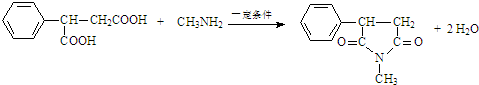 .
.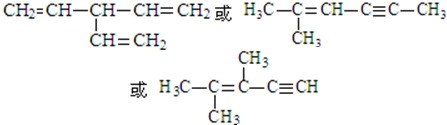 (写出一种即可).
(写出一种即可).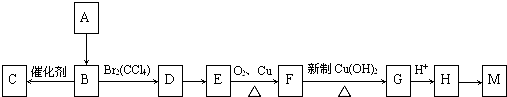
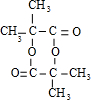 .
.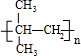 ;E→F:2(CH3)2C(OH)-CH2OH+O2$→_{△}^{Cu}$2(CH3)2C(OH)-CHO+2H2O.
;E→F:2(CH3)2C(OH)-CH2OH+O2$→_{△}^{Cu}$2(CH3)2C(OH)-CHO+2H2O.