题目内容
9.下列说法不正确的是( )| A. | 加热氯化铁溶液,溶液颜色变深与盐类水解有关 | |
| B. | NaHS溶液水解方程式为:HS-+H2O?H2S+OH- | |
| C. | Na2SO3溶液中,c(OH-)=c(H+)+c(HSO3-)+c(H2SO3) | |
| D. | 0.1 mol•L-1的CH3COOH溶液和0.1 mol•L-1的CH3COONa溶液等体积混合:c(CH3COO-)+c(CH3COOH)=2c(Na+) |
分析 A、三价铁水解受温度的影响,温度越高水解程度越大;
B、HS-是弱酸根,在溶液中会水解;
C、根据Na2SO3溶液中的质子守恒来分析;
D、根据混合溶液中的物料守恒来分析.
解答 解:A、三价铁水解受温度的影响,温度越高水解程度越大,生成的氢氧化铁越多,颜色变深,与盐类水解有关,故A正确;
B、HS-是弱酸根,在溶液中会结合水电离出的氢离子而水解:HS-+H2O?H2S+OH-,故B正确;
C、Na2SO3溶液中所有的H+和所有的OH-均来自于水,而SO32-的水解时会将部分H+结合为HSO3-和H2SO3,故根据电荷守恒来列式有:c(OH-)=c(H+)+c(HSO3-)+2c(H2SO3),故C错误;
D、0.1 mol•L-1的CH3COOH溶液和0.1 mol•L-1的CH3COONa溶液等体积混合后,所得的是浓度均为0.05mol/L的CH3COOH和CH3COONa的混合溶液,根据物料守恒可有:c(CH3COO-)+c(CH3COOH)=2c(Na+),故D正确.
故选.
点评 本题考查了盐溶液的水解以及三个守恒的应用,综合性较强,难度适中.

练习册系列答案
 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
2.全世界每年因钢铁锈蚀造成大量的损失.某学生欲探究在蒸馏水、氯化钠溶液和醋酸溶液三种条件下铁锈蚀的快慢,设计了如下实验.
请回答:
①在一周的观察过程中,他发现实验序号为II的试管中铁钉锈蚀速度最慢.
②下列防止钢铁锈蚀的措施不合理的是C(填字母).
A.在自行车的钢圈表面镀镍
B.改变金属内部结构制成不锈钢.
C.在地下钢铁管道上连接铜块
③炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会因腐蚀出现红褐色锈斑.试回答:铁锅的腐蚀主要是由电化学腐蚀造成的.
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 实验 内容 | 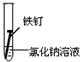 | 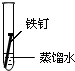 | 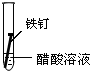 |
①在一周的观察过程中,他发现实验序号为II的试管中铁钉锈蚀速度最慢.
②下列防止钢铁锈蚀的措施不合理的是C(填字母).
A.在自行车的钢圈表面镀镍
B.改变金属内部结构制成不锈钢.
C.在地下钢铁管道上连接铜块
③炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会因腐蚀出现红褐色锈斑.试回答:铁锅的腐蚀主要是由电化学腐蚀造成的.
14.如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为23.下列说法正确的是( )
| X | Y | ||
| Z | W | ||
| T |
| A. | X、Y、Z三种元素最低价氢化物的沸点依次升高 | |
| B. | 由X、Y和氢三种元素形成的化合物中只有共价键 | |
| C. | 含Z元素的弱酸不能与含W元素的弱酸反应得到强酸 | |
| D. | T元素形成的酸与W元素形成的酸相比,酸性一定后者弱 |
1.表是元素周期表的一部分,Y原子最外层电子数是次外层电子数的3倍,下列说法正确的是( )
| X | Y | ||
| M | Z |
| A. | 简单氢化物稳定性:X>Z | B. | 简单离子半径:Y<M | ||
| C. | 最高价氧化物水化物的酸性:Z<M | D. | 得电子能力:X>Y |
19.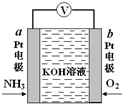 电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质.下列说法错误的是( )
电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质.下列说法错误的是( )
 电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质.下列说法错误的是( )
电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质.下列说法错误的是( )| A. | 溶液中OH-向电极a移动 | |
| B. | 反应消耗的NH3与O2的物质的量之比为4:5 | |
| C. | O2在电极b上发生还原反应 | |
| D. | 负极的电极反应式为:2NH3-6e-+6OH-=N2↑+6H2O |

 ;
; 、和
、和 ;
; .
.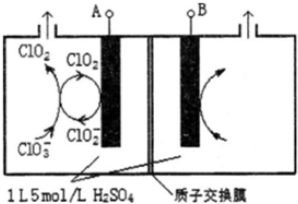 研究含Cl、N、S等元素的化合物对净化水质、防治污染有重要意义.
研究含Cl、N、S等元素的化合物对净化水质、防治污染有重要意义.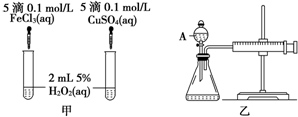 (1)下列反应属于吸热反应的是DE
(1)下列反应属于吸热反应的是DE 氨是重要的化工原料,用途很广.
氨是重要的化工原料,用途很广.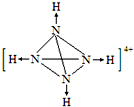 .
.