题目内容
5.分子式为C4H8O3的有机物,在一定条件下具有下列性质:①在浓硫酸存在下,能分别与CH3CH2OH或CH3COOH反应;②在浓硫酸存在下,亦能脱水生成一种只存在一种结构形式,且能使溴水褪色的物质;③在浓硫酸存在下,还能生成一种分子式为C4H6O2的五元环状化合物.根据上述性质,确定C4H8O3的结构简式为( )| A. | HOCH2COOCH2CH3 | B. | CH3CH(OH)CH2COOH | C. | HOCH2CH2CH2COOH | D. | CH3CH2CH(OH)COOH |
分析 ①在浓硫酸存在下,能分别与CH3CH2OH或CH3COOH反应,说明分子中含有-OH和-COOH;
②在浓硫酸存在下,能发生消去反应且只有一种有机产物,说明生成生成一种位置的C=C;
③在浓硫酸存在下,还能生成一种分子式为C4H6O2的五元环状化合物.
根据以上信息结合选项中的有机物的结构判断.
解答 解:①在浓硫酸存在下,能分别与CH3CH2OH或CH3COOH反应,说明分子中含有-OH和-COOH;
②在浓硫酸存在下,能发生消去反应且只有一种有机产物,说明生成生成一种位置的C=C;
③在浓硫酸存在下,还能生成一种分子式为C4H6O2的五元环状化合物.
A.在浓硫酸存在下,不能发生消去反应,故A错误;
B.发生消去反应生成两种有机物,故B错误;
C.消去反应只生成一种物质,能形成分子式为C4H6O2的五元环状化合物,故C正确
D.在浓硫酸存在下,发生酯化反应生成三元环状化合物,故D错误;
故选C.
点评 本题考查有机物的推断,题目难度不大,本题注意把握题给信息,为解答该题的关键,做题时注意审题,可用排除法做题.

练习册系列答案
相关题目
15.一定条件下反应A(s)+3B(g)?2C(g)在10L的密闭容器中进行,测得2min内,A的物质的量由20mol(560g)减小到8mol(224g),则下列说法中正确的是( )
| A. | 用反应物A表示该反应的反应速率为0.6 mol•L-1•min-1 | |
| B. | 用反应物B表示该反应的反应速率为2.4 mol•L-1•min-1 | |
| C. | 2v(B)=3v(C) | |
| D. | 用生成物C表示该反应的反应速率为3.6 mol•L-1•min-1 |
20.根据反应:2Ag++Cu═Cu2++2Ag,设计如图所示原电池,下列说法错误的是( )
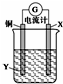

| A. | X可以是银或石墨 | B. | 电子从铜电极经外电路流向X电极 | ||
| C. | Y是硫酸铜溶液 | D. | X极上的电极反应式为Ag++e-═Ag |
10.部分中学化学常见元素原子结构及性质如表所示:
(1)A原子在周期表中的位置为第四周期Ⅷ族.
(2)B与C形成的化合物的化学式为Mg3N2.
(3)F与E可以形成原子个数比分别为2:1、1:1的两种化合物X和Y,区别X与Y的水溶液的实验方法是分别取X、Y各少许置于试管中,再各加入少量的MnO2粉末,迅速产生无色气体的是H2O2,无明显现象的是H2O.
(4)C与E都是较活泼的非金属元素,用化学方程式表明这两种单质的氧化性强弱4NH3+3O2(纯)$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O.
| 序号 | 元素 | 结构及性质 |
| ① | A | A单质是生活中常见金属,它有两种氯化物,相对分子质量相差35.5 |
| ② | B | B原子最外层电子数是内层电子总数的$\frac{1}{5}$ |
| ③ | C | C是常见化肥的主要元素,单质常温下呈气态 |
| ④ | D | D单质被誉为“信息革命的催化剂”,是常用的半导体材料 |
| ⑤ | E | 通常情况下,E没有正化合价,A、B、C、D、F都能与E形成化合物 |
| ⑥ | F | F在周期表中可以排在ⅠA族,也有人提出排在ⅦA族 |
(2)B与C形成的化合物的化学式为Mg3N2.
(3)F与E可以形成原子个数比分别为2:1、1:1的两种化合物X和Y,区别X与Y的水溶液的实验方法是分别取X、Y各少许置于试管中,再各加入少量的MnO2粉末,迅速产生无色气体的是H2O2,无明显现象的是H2O.
(4)C与E都是较活泼的非金属元素,用化学方程式表明这两种单质的氧化性强弱4NH3+3O2(纯)$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O.
17.关于原电池的下列说法中,正确的是( )
| A. | 化学性质较活泼的金属为负极 | B. | 在正极上发生氧化反应 | ||
| C. | 在外电路,电子流出的极为正极 | D. | 是由电能转化为化学能的装置 |

 已知A为金属单质,根据下列变化完成以下问题:
已知A为金属单质,根据下列变化完成以下问题: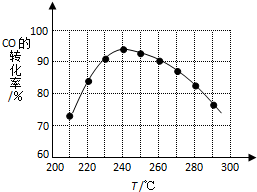 二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用.工业上以CO和H2为原料生产CH3OCH3的新工艺主要发生三个反应:
二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用.工业上以CO和H2为原料生产CH3OCH3的新工艺主要发生三个反应: