题目内容
20.根据反应:2Ag++Cu═Cu2++2Ag,设计如图所示原电池,下列说法错误的是( )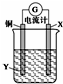
| A. | X可以是银或石墨 | B. | 电子从铜电极经外电路流向X电极 | ||
| C. | Y是硫酸铜溶液 | D. | X极上的电极反应式为Ag++e-═Ag |
分析 由方程式2Ag++Cu═Cu2++2Ag可知,反应中Ag+被还原,应为正极反应,则电解质溶液为硝酸银溶液,Cu被氧化,应为原电池负极反应,在装置图中X为Ag或石墨,Y为硝酸银溶液,以此解答该题.
解答 解:A.铜为负极,电极X的材料是Ag或石墨,为原电池的正极,故A正确;
B.原电池工作时,电子从负极(铜)经外电路流向X电极(银或石墨),故B正确;
C.Y为硝酸银溶液,Ag+被还原,为正极反应,故C错误;
D.X为正极,发生还原反应生成银,极反应式为Ag++e-═Ag,故D正确.
故选C.
点评 本题考查原电池知识,为高考常见题型及高频考点,侧重于学生的分析能力和基本理论的理解和应用能力,难度不大,注意把握电极反应的判断和电极方程式的书写.

练习册系列答案
相关题目
8.下列物质的水溶液能导电,但属于非电解质的是( )
| A. | CH3COOH | B. | Na2O | C. | H2SO4 | D. | SO2 |
5.分子式为C4H8O3的有机物,在一定条件下具有下列性质:①在浓硫酸存在下,能分别与CH3CH2OH或CH3COOH反应;②在浓硫酸存在下,亦能脱水生成一种只存在一种结构形式,且能使溴水褪色的物质;③在浓硫酸存在下,还能生成一种分子式为C4H6O2的五元环状化合物.根据上述性质,确定C4H8O3的结构简式为( )
| A. | HOCH2COOCH2CH3 | B. | CH3CH(OH)CH2COOH | C. | HOCH2CH2CH2COOH | D. | CH3CH2CH(OH)COOH |
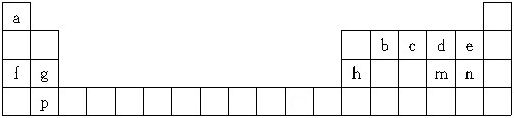
12.A、B、C、D、E是元素周期表中前四周期中五种常见元素,其相关信息如下表:
请回答下列问题:
(1)E在元素周期表中的位置第四周期第Ⅷ族;D原子结构示意图是
(2)B、C、D的简单离子半径由大到小的顺序为(用化学符号表示,下同)S2->O2->Na+,B、D的简单气态氢化物中稳定性较大的是H2O
(3)B、C的单质按物质的量比1:2形成的化合物中化学键的类型为离子键、好几件;该化合物电子式为 .
.
(4)E的一种具有磁性的黑色晶体发生铝热反应的化学方程式是3Fe3O4+8Al$\frac{\underline{\;高温\;}}{\;}$9Fe+4Al2O3.
| 元素 | 相关信息 |
| A | 原子核外L层电子数是K层的2倍 |
| B | 其一种单质被称为地球生物的“保护伞” |
| C | 焰色反应呈黄色 |
| D | 与B同主族的短周期元素 |
| E | 可形成多种氧化物,其中一种为具有磁性的黑色晶体 |
(1)E在元素周期表中的位置第四周期第Ⅷ族;D原子结构示意图是

(2)B、C、D的简单离子半径由大到小的顺序为(用化学符号表示,下同)S2->O2->Na+,B、D的简单气态氢化物中稳定性较大的是H2O
(3)B、C的单质按物质的量比1:2形成的化合物中化学键的类型为离子键、好几件;该化合物电子式为
 .
.(4)E的一种具有磁性的黑色晶体发生铝热反应的化学方程式是3Fe3O4+8Al$\frac{\underline{\;高温\;}}{\;}$9Fe+4Al2O3.
9.下列叙述I和II均正确并有因果关系的是( )
| 选项 | 叙述I | 叙述II |
| A | Mg有还原性 | 电解MgCl2饱和溶液可制备Mg |
| B | AgCl难溶于酸 | 用盐酸和AgNO3溶液检验Cl- |
| C | Ba(OH)2易溶于水 | 可配制1.0mol?L-1的Ba(OH)2溶液 |
| D | NH4Cl为强酸弱碱盐 | 用加热法除去NaCl中的NH4Cl |
| A. | A | B. | B | C. | C | D. | D |
11.一定温度下,在三个体积约为2.0L的恒容密闭容器中发生反应:2CH3OH(g)=CH3OCH3(g)+H2O(g)
回答下列问题:
(1)反应的△H小于0(填“大于”或“小于”)判断的理由是反应Ⅰ、Ⅲ起始量相同,Ⅰ的CH3OCH3(g)含量低,说明降温正向移动,正反应为放热过程△H<0,容器Ⅰ到达平衡所需的时间为20min反应速率v(CH2OH)为0.004mol•L-1•min-1,列式求算387℃时该反应的平衡常数K1=4
(2)容器Ⅱ达平衡时,压强是容器Ⅰ的两倍,CH3OH的体积分数和容器Ⅰ中的相同,CH3OH起始的物质的量为0.40mol;平衡时CH3OCH3(g)的体积分数为0.4
(3)t分钟后容器Ⅲ达到平衡,t大于20min(填“大于”、“等于”或“小于”)判断的理由是温度越低,反应速率越小,达到平衡时所需的时间越长请在图中分别画出容器Ⅰ和容器Ⅱ中CH3OH(g)浓度变化的曲线示意图

(4)208℃,若向3L容器中充入0.9molCH3OH(g),0.6molCH3OCH3(g)和0.3molH2O(g),则起始时该反应的v正>v逆(填“>”“<”或“=”)
| 容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| Ⅰ | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 387 | |||
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
(1)反应的△H小于0(填“大于”或“小于”)判断的理由是反应Ⅰ、Ⅲ起始量相同,Ⅰ的CH3OCH3(g)含量低,说明降温正向移动,正反应为放热过程△H<0,容器Ⅰ到达平衡所需的时间为20min反应速率v(CH2OH)为0.004mol•L-1•min-1,列式求算387℃时该反应的平衡常数K1=4
(2)容器Ⅱ达平衡时,压强是容器Ⅰ的两倍,CH3OH的体积分数和容器Ⅰ中的相同,CH3OH起始的物质的量为0.40mol;平衡时CH3OCH3(g)的体积分数为0.4
(3)t分钟后容器Ⅲ达到平衡,t大于20min(填“大于”、“等于”或“小于”)判断的理由是温度越低,反应速率越小,达到平衡时所需的时间越长请在图中分别画出容器Ⅰ和容器Ⅱ中CH3OH(g)浓度变化的曲线示意图

(4)208℃,若向3L容器中充入0.9molCH3OH(g),0.6molCH3OCH3(g)和0.3molH2O(g),则起始时该反应的v正>v逆(填“>”“<”或“=”)
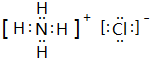 .
.