题目内容
16.水是生命之源,它与我们的生活密切相关.在化学实验和科学研究中,水也是一种常用的试剂.(1)水分子中氧原子在基态时核外电子排布式为1s22s22p4;
(2)写出与H2O分子互为等电子体的微粒H2S、NH2-(填2种).
(3)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+).下列对上述过程的描述不合理的是A.
A.氧原子的杂化类型发生了改变 B.微粒的形状发生了改变
C.微粒的化学性质发生了改变 D.微粒中的键角发生了改变
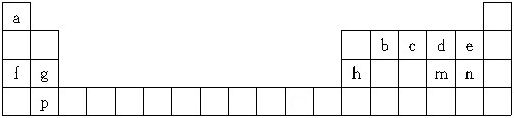
(4)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序).与冰的晶体类型相同的是BC(请用相应的编号填写)

(5)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51kJ/mol,除氢键外,水分子间还存在范德华力(11kJ/mol),则冰晶体中氢键的“键能”是20kJ/mol.
分析 (1)根据O原子核外有8个电子,据此分析解答;
(2)根据原子数目和价电子数目来分析等电子体;
(3)水中氧的杂化为sp3,H3O+中氧的杂化为sp3,据此解答;
(4)冰属于分子晶体,利用晶胞图来判断晶体的构成微粒,以此来分析;
(5)升华热=范德华力+氢键,利用均摊法计算水分子与氢键的关系,结合升华热、范德华力计算氢键键能.
解答 解:(1)水分子中氧原子的核外电子数为8,氧原子在基态时核外电子排布式为1s22s22p4,故答案为:1s22s22p4;
(2)H2O分子中的原子数为3,价电子数为10,H2S、NH2-的原子数目均为3,价电子数目均为10,则与水互为等电子体,故答案为:H2S、NH2-;
(3)A.水中氧的杂化为sp3,H3O+中氧的杂化为sp3,则氧原子的杂化类型没有改变,故A错误;
B.水分子为V型,H3O+为三角锥型,则微粒的形状发生了改变,故B正确;
C.因结构不同,则性质不同,微粒的化学性质发生了改变,故C正确;
D.水分子为V型,H3O+为三角锥型,微粒中的键角发生了改变,故D正确;
故答案为:A;
(4)冰属于分子晶体,由晶胞图可知,B为干冰的晶胞图,构成微粒为分子,C为碘的晶胞图,构成微粒为碘分子,则与冰的晶体类型相同的是BC,故答案为:BC;
(5)冰的升华热是51kJ/mol,水分子间还存在范德华力(11kJ/mol),根据图象知,1mol水中含有2mol氢键,升华热=范德华力+氢键,所以冰晶体中氢键的“键能”是20kJ/mol,故答案为:20.
点评 本题考查了晶胞的计算、电子排布图的书写等知识点,难点是计算氢键的键能,会运用均摊法计算晶胞是解本题的关键,难度较大.

练习册系列答案
相关题目
6.一种新型燃料电池,以镍板为电极插入KOH溶液中,分别向两极通乙烷和氧气,电极反应为:C2H6+18OH--14e-═2CO${\;}_{3}^{2-}$+12H20;7H2O+$\frac{7}{2}$O2+14e-═14OH-.有关此电池的推断错误的是( )
| A. | 通乙烷的电极为负极 | |
| B. | 参加反应的O2与C2H6的物质的量之比为7:2 | |
| C. | 放电一段时间后,KOH的物质的量浓度将下降 | |
| D. | 在电解质溶液中CO${\;}_{3}^{2-}$向正极移动 |
7.在0.1mol•L-1的CH3COOH溶液中存在CH3COOH?CH3COO-+H+电离平衡,对于该平衡下列叙述正确的是( )
| A. | 加入少量Na2CO3固体,平衡不移动 | |
| B. | 加大量的水后,反应速率增大,平衡向逆反应方向移动 | |
| C. | 加入少量NaOH固体,平衡向正反应方向移动 | |
| D. | 滴加少量0.1 mol•L-1HCl溶液,溶液中c(H+)减少 |
8.下列物质的水溶液能导电,但属于非电解质的是( )
| A. | CH3COOH | B. | Na2O | C. | H2SO4 | D. | SO2 |
5.分子式为C4H8O3的有机物,在一定条件下具有下列性质:①在浓硫酸存在下,能分别与CH3CH2OH或CH3COOH反应;②在浓硫酸存在下,亦能脱水生成一种只存在一种结构形式,且能使溴水褪色的物质;③在浓硫酸存在下,还能生成一种分子式为C4H6O2的五元环状化合物.根据上述性质,确定C4H8O3的结构简式为( )
| A. | HOCH2COOCH2CH3 | B. | CH3CH(OH)CH2COOH | C. | HOCH2CH2CH2COOH | D. | CH3CH2CH(OH)COOH |
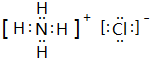 .
.
 ;
;