题目内容
18.某研究性学习小组为测定某铝镁合金(不含其他元素)中镁的质量分数,设计了下列两种不同实验方案进行探究,请根据他们的设计回答有关问题.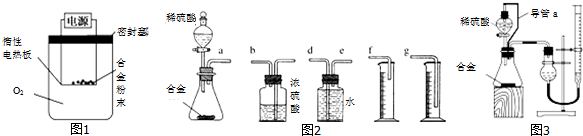
[探究一]实验方案:称量x g铝镁合金粉末,放在如图1所示装置的惰性电热板上,通电使其充分灼烧.(密封装置中氧气足量)
问题讨论:
(1)欲计算Mg的质量分数,该实验中还需测定的数据是铝镁合金充分灼烧后的固体质量.
(2)假设实验中测出该数据为y g,则原铝镁合金粉末中镁的质量分数为$\frac{17x-9y}{2x}$×100%(用含x、y的代数式表示).
[探究二]实验方案:称量x g铝镁合金粉末溶于稀硫酸,常温下测定生成气体的体积.
问题讨论:
(3)同学们拟选用如图2的实验装置完成实验,你认为最简易的装置的连接顺序是a接e,,d接g,.接..(填接口字母,空格不一定填完,不够可加).
(4)同学们仔细分析(3)题中连接的实验装置后,又设计了如图3所示的实验装置.
①装置中导管a的作用是便于分液漏斗中稀硫酸顺利流出(或平衡分液漏斗与锥形瓶中气压)
②反应结束后发现量气管的液面高于干燥管的液面,此时应如何操作?(待产生H2恢复至室温时,)仅将量气管慢慢下移至液面与干燥管中液面相平
③与图3装置相比,用图2连接的装置进行实验时,若不考虑导管中液体体积的影响,测定铝镁合金中镁的质量分数将偏小(填“偏大”、“偏小”或“无影响”).
分析 探究一实验原理为:铝镁合金粉末与氧气充分反应生成镁和铝的氧化物,根据铝镁的质量和氧化后的氧化物的质量通过列方程组法可以求得镁、铝的各自的质量,据此计算和分析;
探究二实验原理为:利用铝镁合金粉末与足量的盐酸反应,测定产生氢气的体积,根据铝镁合金粉末的质量与产生氢氧的总体积列方程组可求得镁、铝的各自的质量,
(3)根据实验原理可知,装置的组装顺序:合金与稀硫酸反应,用排水量气法测定氢气的体积,其中盛水的试剂瓶导管一定要短进长出,增大压强原理将水排出,量筒中水的体积就是生成氢气的体积,量筒内导管应伸入量筒底部;
(4)①保持分液漏斗内气体压强与锥形瓶内气体压强相等,打开分液漏斗活塞时稀硫酸能顺利滴下,滴入锥形瓶的稀硫酸体积等于进入分液漏斗的气体体积,从而消除由于加入稀硫酸引起的氢气体积误差;
②为了准确测定氢气的体积,量气管的液面与干燥管的液面必须水平相齐,如果不等,可以通过调节量气管的高度使液面水平相齐;
③与图3装置相比,用图2连接的装置进行实验时,稀硫酸放入锥形瓶中会使收集到的氢气的体积偏大,图3中用了导管a消除了稀硫酸的体积对氢气体积的影响,据此分析.
解答 解:探究一实验原理为:铝镁合金粉末与氧气充分反应生成镁和铝的氧化物,根据铝镁的质量和氧化后的氧化物的质量通过列方程组法可以求得镁、铝的各自的质量,
(1)根据上面的分析可知,欲计算Mg的质量分数,该实验中还需测定的数据是铝镁合金充分灼烧后的固体质量,
故答案为:铝镁合金充分灼烧后的固体质量;
(2)设铝镁合金粉末中镁的质量a,铝的质量为b,则根据反应可知产生的氧化铝的质量为$\frac{102}{54}$b=$\frac{51}{27}$b,氧化镁的质量为$\frac{40}{24}$a=$\frac{5}{3}$a,则题意得$\left\{\begin{array}{l}{a+b=x}\\{\frac{51}{27}b+\frac{5}{3}a=y}\end{array}\right.$,解得a=$\frac{17x-9y}{2}$,所以原铝镁合金粉末中镁的质量分数为$\frac{a}{x}$×100%=$\frac{17x-9y}{2x}$×100%,
故答案为:$\frac{17x-9y}{2x}$×100%;
探究二实验原理为:利用铝镁合金粉末与足量的盐酸反应,测定产生氢气的体积,根据铝镁合金粉末的质量与产生氢氧的总体积列方程组可求得镁、铝的各自的质量,
(3)根据实验原理可知,装置的组装顺序:合金与水反应,用排水量气法测定氢气的体积,其中盛水的试剂瓶导管一定要短进长出,利用增大压强原理将水排出,量筒中水的体积就是生成氢气的体积,量筒内导管应伸入量筒底部,故连接顺序为:(a)接(e)、(d)接(g),
故答案为:e,d、g;
(4)①装置中导管a的作用是:保持分液漏斗内气体压强与锥形瓶内气体压强相等,打开分液漏斗活塞时稀硫酸能顺利滴下,滴入锥形瓶的稀硫酸体积等于进入分液漏斗的气体体积,从而消除由于加入稀硫酸引起的氢气体积误差,
故答案为:便于分液漏斗中稀硫酸顺利流出(或平衡分液漏斗与锥形瓶中气压);
②为了准确测定氢气的体积,量气管的液面与干燥管的液面必须水平相齐,如果不等,可以通过调节量气管的高度使液面水平相齐,所以如果发现量气管的液面高于干燥管的液面,可以(待产生H2恢复至室温时,)将量气管慢慢下移至液面与干燥管中液面相平,
故答案为:(待产生H2恢复至室温时,)将量气管慢慢下移至液面与干燥管中液面相平;
③图3中用了导管a消除了稀硫酸的体积对氢气体积的影响,与图3装置相比,用图2连接的装置进行实验时,稀硫酸放入锥形瓶中会使收集到的氢气的体积偏大,所以通过计算得到的铝的质量分数偏大,镁的质量分数偏小,
故答案为:偏小.
点评 主要考查物质含量的测定、对实验原理与装置的理解、实验方案设计等,难度中等,理解实验原理是解题的关键,是对知识的综合考查,需要学生具有知识的基础与综合运用知识分析问题、解决问题的能力.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案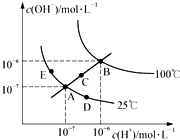
| A. | 图中五点的KW间的关系为:B>C>A=D=E | |
| B. | 若从A点到D点,可采用:恒温条件下,在水中加入少量的醋酸,提高溶液酸性 | |
| C. | 若从A点到C点,可采用:恒温条件下,在水中加入少量的醋酸铵,促进水的电离 | |
| D. | 100℃时,将pH=2的硫酸与0.01mol•L-1的KOH溶液等体积混合后,溶液中c(H+)=c(OH-)=10-6mol•L-1 |
 在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)?M(g)+N(g)所得实验数据如表:
在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)?M(g)+N(g)所得实验数据如表:| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(X) | n(Y) | n(M) | ||
| ① | 700 | 0.40 | 0.10 | 0.090 |
| ② | 800 | 0.10 | 0.40 | 0.080 |
| ③ | 800 | 0.20 | 0.30 | a |
| ④ | 900 | 0.10 | 0.15 | b |
(1)实验①中,若5min时测得,n(M)=0.050mo1,则0至5min时间内,用N表示的平均反应速率为1.0×10-3mol/(L•min).
(2)实验③平衡常数为1.0,该正反应为放热反应(填“吸热”或“放热”)
(3)能说明上述反应一定达到平衡的条件是C.
A.c(Y)=c(N) B.平均分子量不再变化
C.v正(X)=v逆(M) D.温度和压强一定时,混合气体的密度不再变化
(4)实验③中,达到平衡时,X的转化率为60%多余.
(5)实验③、④中,达到平衡时,a与b的关系为A(填选项),请解释原因若温度不变,则b=$\frac{1}{2}$a,该反应为放热反应,温度升高,平衡向逆反应方向移动,故b<$\frac{1}{2}$a,即a>2b.
A.a>2b B.a=2b C.b<a<2b D.a<b
(6)如图是实验①中c(M)随时间变化的曲线图,请在图中画出实验②中c(M)随时间变化的曲线图.
| A. | (b-a)g | B. | (b-a)×ωg | C. | ($\frac{53b}{143}$-a)g | D. | ($\frac{53b}{143}$-a)×ω%g |
| A. | 能溶于水 | |
| B. | 常温下,0.1 mol•Lˉ1醋酸溶液中的c(H+)为1.32×10-3mol•Lˉ1 | |
| C. | 能使紫色石蕊试液变红 | |
| D. | 能被弱碱氨水中和 |
| A. | 焰火的五彩缤纷是某些金属元素化学性质的展现 | |
| B. | 将煤气化后再作为能源,可减少PM2.5引起的危害 | |
| C. | 石英用于生产光导纤维和计算机芯片 | |
| D. | 包装食品里常有硅胶、石灰、还原铁粉三类小包,其作用相同 |
| A. | Al2(SO4)3═3Al3++2SO42- | B. | AlCl3═Al3++Cl3- | ||
| C. | Mg(NO3)2═Mg2++2NO3- | D. | KMnO4═K++Mn2++4O2- |