题目内容
8.下列电离方程式,书写正确的是( )| A. | Al2(SO4)3═3Al3++2SO42- | B. | AlCl3═Al3++Cl3- | ||
| C. | Mg(NO3)2═Mg2++2NO3- | D. | KMnO4═K++Mn2++4O2- |
分析 A.原子个数不守恒;
B.氯离子书写错误;
C.硝酸镁为强电解质,完全电离;
D.高锰酸钾为强电解质,完全电离生成钾离子与高锰酸根离子.
解答 解:A.硫酸铝为强电解质,电离方程式:Al2(SO4)3═2Al3++3SO42-,故A错误;
B.氯化铝为强电解质,完全电离,电离方程式:AlCl3═Al3++3Cl-,故B错误;
C.硝酸镁为强电解质,完全电离,电离方程式:Mg(NO3)2═Mg2++2NO3-,故C正确;
D.高锰酸钾为强电解质,完全电离生成钾离子与高锰酸根离子,电离方程式:KMnO4═K++MnO4-,故D错误;
故选:C.
点评 本题考查了电解质电离方程式的书写,明确电解质强弱、电离方程式书写方法是解题关键,注意电离方程式遵循原子个数守恒、电荷数守恒规律,题目难度不大.

练习册系列答案
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
19.氢气是一种清洁能源,氢气的制取是氢能源利用领域的研究热点.
(1)纳米级的Cu2O可作为太阳光分解水的催化剂.一定温度下,在2L密闭容器中加入纳米级Cu2O并通入0.10mol水蒸气发生反应:2H2O(g)$?_{Cu_{2}O}^{光照}$2H2(g)+O2(g)△H=+484kJ•mol-1,不同时段产生O2的量见下表:
上述反应过程中能量转化形式为光能转化为化学能,达平衡过程中至少需要吸收光能为0.968kJ.
(2)现有反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H<0,在相同温度和相同体积下进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表:
上述四种情况达到平衡后,甲、乙、丙、丁容器中n(CO)的大小顺序为丁>乙>甲=丙.
(3)金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝.高温下,在密闭容器中用H2还原WO3得金属钨,总反应为WO3 (s)+3H2 (g)$\stackrel{高温}{?}$W (s)+3H2O (g).请回答下列问题:
①某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为60%.
②上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
假设WO3完全转化为W,则三个阶段消耗H2物质的量之比为1:1:4.
③钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W(s)+2I2 (g)$?_{3000℃}^{1400℃}$ WI4 (g).下列说法正确的有AB(填字母).
A.灯管内的I2可循环使用
B.WI4在灯丝上分解,产生的W又沉积在灯丝上
C.WI4在灯管壁上分解,使灯管的寿命延长
D.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢.
(1)纳米级的Cu2O可作为太阳光分解水的催化剂.一定温度下,在2L密闭容器中加入纳米级Cu2O并通入0.10mol水蒸气发生反应:2H2O(g)$?_{Cu_{2}O}^{光照}$2H2(g)+O2(g)△H=+484kJ•mol-1,不同时段产生O2的量见下表:
| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
(2)现有反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H<0,在相同温度和相同体积下进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表:
| 物质的量 | CO | H2 O | CO2 | H2 |
| 甲 | a mol | a mol | 0mol | 0mol |
| 乙 | 0mol | 0mol | 2a mol | a mol |
| 丙 | 0mol | 0mol | a mol | a mol |
| 丁 | a mol | a mol | a mol | a mol |
(3)金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝.高温下,在密闭容器中用H2还原WO3得金属钨,总反应为WO3 (s)+3H2 (g)$\stackrel{高温}{?}$W (s)+3H2O (g).请回答下列问题:
①某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为60%.
②上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
| 温度 | 25℃~550℃~600℃~700℃ |
| 主要成份 | WO3 W2O5 WO2 W |
③钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W(s)+2I2 (g)$?_{3000℃}^{1400℃}$ WI4 (g).下列说法正确的有AB(填字母).
A.灯管内的I2可循环使用
B.WI4在灯丝上分解,产生的W又沉积在灯丝上
C.WI4在灯管壁上分解,使灯管的寿命延长
D.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢.
16.已知:Fe(OH)3不溶于过量氨水,Cu(OH)2溶于过量氨水,转化为[Cu(NH3)4]2+.现有等物质的量组成的铁铜合金0.1mol,研成粉末后,全部投入稀硝酸中,微热使其充分反应,硝酸的还原产物只有NO.由于HNO3用量的不同,溶液中的金属离子和残留固体的成分会有多种情况.下列说法正确的是( )
| A. | 根据溶液中的金属离子和残留固体的成分最多会有6种情况 | |
| B. | 若金属有剩余,在溶液中再滴入稀硫酸后,金属不会再溶解 | |
| C. | 当合金刚好溶解时,在标准状况下产生2.24LNO | |
| D. | 若合金全部溶解,在溶液中加入过量的氨水,经过滤、洗涤、干燥、充分灼烧、称量得固体5.35g |
3.下列说法正确的是(NA为阿伏加德罗常数)( )
| A. | 28g氮气含有的原子数为NA | |
| B. | 32 g O2中所含的氧原子数目为2NA | |
| C. | 2.7g金属铝与足量盐酸反应时失去的电子数为0.1NA | |
| D. | 标准状况下22.4L水所含的分子数为NA |
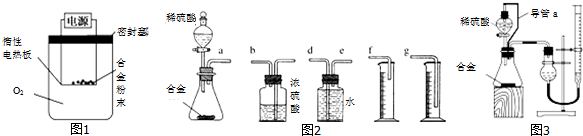
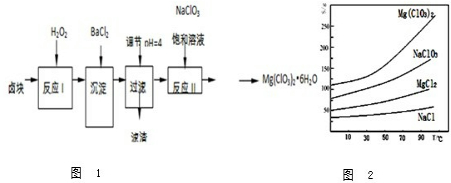

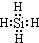 .
.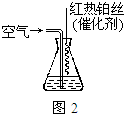 (2)三硅酸镁(Mg2Si3O8?nH2O)难溶于水,在医药上可做抗酸剂.它除了可以中和胃液中多余酸之外,生成的H2SiO3还可覆盖在有溃疡的胃表面,保护其不再受刺激.三硅酸镁与盐酸反应的化学方程式为Mg2Si3O8?nH2O+4HCl═2MgCl2+3H2SiO3+(n-1)H2O.
(2)三硅酸镁(Mg2Si3O8?nH2O)难溶于水,在医药上可做抗酸剂.它除了可以中和胃液中多余酸之外,生成的H2SiO3还可覆盖在有溃疡的胃表面,保护其不再受刺激.三硅酸镁与盐酸反应的化学方程式为Mg2Si3O8?nH2O+4HCl═2MgCl2+3H2SiO3+(n-1)H2O.