��Ŀ����
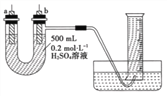
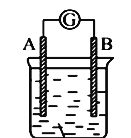
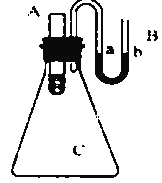
����Ŀ���������ƿ������Ʊ������ᣮ�Ծ�����ˮ��Ϊԭ���Ʊ��������ƾ��壨NaClO4H2O�����������£� 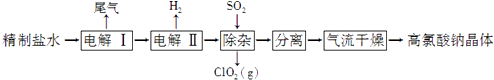
��1���ɴ��Σ���Ca2+��Mg2+�� ![]() ��Br�������ʣ��Ʊ�������ˮʱ���õ�NaOH��BaCl2��Na2CO3���Լ���Na2CO3������������ȥ��ˮ�е�Br�����Խ�ʡ�������еĵ��ܣ���ԭ���� ��
��Br�������ʣ��Ʊ�������ˮʱ���õ�NaOH��BaCl2��Na2CO3���Լ���Na2CO3������������ȥ��ˮ�е�Br�����Խ�ʡ�������еĵ��ܣ���ԭ���� ��
��2��������Ŀ�����Ʊ�NaClO3��Һ��������β����H2�⣬���������ѧʽ���������Ļ�ѧ����ʽΪ ��
��3�������ӡ���Ŀ���dz�ȥ������NaClO3���ʣ��÷�Ӧ�����ӷ���ʽΪ �� ���������ʱ���¶ȿ�����80��100���ԭ���� ��
���𰸡�
��1����ȥCa2+�������Ba2+�����ʱBr��������
��2��Cl2��NaClO3+H2O ![]() NaClO4+H2��
NaClO4+H2��
��3��2ClO3��+SO2�T2ClO2+SO42�����¶�̫�ߣ��������ƾ���ʧȥ�ᾧˮ��ֽ⣻�¶�̫�ͣ����ﲻ���
���������⣺��1��Na2CO3��������̼�������������Ӻͳ��������������ı����ӷ������ֽⷴӦ���������ܵ�̼��ƺ�̼�ᱵ������̼���Ƶ�����Ϊ��ȥ�����Ӻͱ����ӣ�Br���Ļ�ԭ��ǿ�������ӣ����Ե����������������ȱ��������ʴ�Ϊ����ȥCa2+�������Ba2+�����ʱBr������������2�������������������ӷŵ磬��Ҫ������������ӣ����ֲ��������������������ӷŵ磬��������������β������������������������������������������ŵ����ɸ����������������ˮ��������������ӷŵ磬�������������Ե�ⷴӦ����ʽΪ��NaClO3+H2O ![]() NaClO4+H2�����ʴ�Ϊ��Cl2��NaClO3+H2O
NaClO4+H2�����ʴ�Ϊ��Cl2��NaClO3+H2O ![]() NaClO4+H2������3����ͼʾ��֪ͨ����������ȥ���е���������ӣ���Ӧ�����ӷ���ʽΪ��2ClO3��+SO2�T2ClO2+SO42�� �� �����¶�̫�Ͳ����ڸ���¶ȹ��߾���Ҫʧˮ���¶�̫�������ƿ��ֽܷ⣬�ʴ�Ϊ��2ClO3��+SO2�T2ClO2+SO42�����¶�̫�ߣ��������ƾ���ʧȥ�ᾧˮ��ֽ⣻�¶�̫�ͣ����ﲻ��֣� ��ԭ���Ȼ��Ƶ��������ƾ��壬�ȵĻ��ϼ����ߣ�������������δ��ǿ������������ͨ�����ʵ�����ȵIJ�ͬ��̬��ת���������̼�Ϊ������ԭ��Ӧ�������Ƶõ���ˮһ�ε����������ƣ��õ�����������Һ������һ�ε�⣬���ɸ������ƣ�Ȼ��ͨ����������ȥ���е������ƣ������з����ᴿ�õ��������ƾ��壬��1��Na2CO3��������̼�������������Ӻͳ��������������ı����ӷ������ֽⷴӦ���������ܵ�̼��ƺ�̼�ᱵ��Br���Ļ�ԭ��ǿ�������ӣ����Ե����������������ȱ���������2�������������������ӷŵ磬��Ҫ������������ӣ����ֲ��������������������ӷŵ磬��������������β������������������������������������������ŵ����ɸ����������������ˮ��������������ӷŵ磬�������������Ե�ⷴӦ����ʽΪ��NaClO3+H2O
NaClO4+H2������3����ͼʾ��֪ͨ����������ȥ���е���������ӣ���Ӧ�����ӷ���ʽΪ��2ClO3��+SO2�T2ClO2+SO42�� �� �����¶�̫�Ͳ����ڸ���¶ȹ��߾���Ҫʧˮ���¶�̫�������ƿ��ֽܷ⣬�ʴ�Ϊ��2ClO3��+SO2�T2ClO2+SO42�����¶�̫�ߣ��������ƾ���ʧȥ�ᾧˮ��ֽ⣻�¶�̫�ͣ����ﲻ��֣� ��ԭ���Ȼ��Ƶ��������ƾ��壬�ȵĻ��ϼ����ߣ�������������δ��ǿ������������ͨ�����ʵ�����ȵIJ�ͬ��̬��ת���������̼�Ϊ������ԭ��Ӧ�������Ƶõ���ˮһ�ε����������ƣ��õ�����������Һ������һ�ε�⣬���ɸ������ƣ�Ȼ��ͨ����������ȥ���е������ƣ������з����ᴿ�õ��������ƾ��壬��1��Na2CO3��������̼�������������Ӻͳ��������������ı����ӷ������ֽⷴӦ���������ܵ�̼��ƺ�̼�ᱵ��Br���Ļ�ԭ��ǿ�������ӣ����Ե����������������ȱ���������2�������������������ӷŵ磬��Ҫ������������ӣ����ֲ��������������������ӷŵ磬��������������β������������������������������������������ŵ����ɸ����������������ˮ��������������ӷŵ磬�������������Ե�ⷴӦ����ʽΪ��NaClO3+H2O ![]() NaClO4+H2������3����ͼʾ��֪ͨ����������ȥ���е���������ӣ���Ӧ�����ӷ���ʽΪ��2ClO3��+SO2�T2ClO2+SO42�� �� �����¶�̫�Ͳ����ڸ���¶ȹ��߾���Ҫʧˮ�Խ�Ͽ��Ǹ������Ʊ������ȶ��ԣ�
NaClO4+H2������3����ͼʾ��֪ͨ����������ȥ���е���������ӣ���Ӧ�����ӷ���ʽΪ��2ClO3��+SO2�T2ClO2+SO42�� �� �����¶�̫�Ͳ����ڸ���¶ȹ��߾���Ҫʧˮ�Խ�Ͽ��Ǹ������Ʊ������ȶ��ԣ�

����Ŀ���������ж�����Ԫ�ص����ݣ���֪Be��ԭ�Ӱ뾶Ϊ0.089 nm����
�� | �� | �� | �� | �� | �� | �� | �� | |
ԭ�Ӱ뾶 ��nm�� | 0.074 | 0.160 | 0.152 | 0.110 | 0.099 | 0.186 | 0.075 | 0.082 |
��������ϼ� | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
������ϼ� | 2 | 3 | 1 | 3 |
��1�����Ԫ�ص������ڱ��е�λ����________________������Ԫ�ش���ͬһ�������_________________________������Ԫ�ط��ű�ʾ����
��2���ϱ���ij����Ԫ���γɵĹ��ۻ������У�ÿ��ԭ�Ӷ����������Ϊ8���ӵ��ȶ��ṹ��д�������ʽ��__________________________(��дһ��
��3��Ԫ�آٺ͢����γ����ֻ����д�����н��ȶ��Ļ�������ˮ��Ӧ�����ӷ���ʽ_____________________________________________________��
��4����﮲���������й㷺Ӧ�ã�����ִ�����ϣ�Li2NH�ȣ�����Яʽ��Դ���ϣ�LiCoO2�ȣ�����������Ҫ��ش����⣺
��![]() ��
��![]() ���˷�Ӧ����������壬
���˷�Ӧ����������壬![]() ��
��![]() �������¶Ѽ��ټ�������˵����ȷ����________
�������¶Ѽ��ټ�������˵����ȷ����________
A. ![]() ��
��![]() ��Ϊͬλ�� B.
��Ϊͬλ�� B. ![]() ��
��![]() ����ͬ�ֺ���
����ͬ�ֺ���
C. ![]() ��
��![]() �Ļ�ѧ���ʲ�ͬ D.
�Ļ�ѧ���ʲ�ͬ D. ![]() ��
��![]() ��ͬ������
��ͬ������
������˵������ȷ����_________
A. ���ԣ�Be(OH)2 < LiOH < NaOH < KOH
B. �뾶��K > Na > Li > Li+
C. �����ԣ�Li+ < Na+ < K+ < Rb+ < Cs+
D. �����ԣ�Cs > Rb > K > Na > Li > Be
����Ŀ���ڲ�ͬ�¶��£���2L�ܱ������м���1mol NO��1mol����̿��������Ӧ��
2NO(g)+C(s) ![]() N2(g)+CO2(g) ��H=-213.5kJ/mol���ﵽƽ��ʱ���������£�
N2(g)+CO2(g) ��H=-213.5kJ/mol���ﵽƽ��ʱ���������£�
�¶�/�� | n(����̿)/mol | n(CO2)/mol |
T1 | X | |
T2 | 0.25 |
����˵������ȷ���ǣ� ��
A. T2��ʱ�����÷�Ӧ����10min�ﵽƽ�⣬��Ӧ����v(NO)=0.025mol/(L��min)
B. T1��ʱ�����÷�Ӧ��ƽ�ⳣ��K=9/16�����ƽ��ʱNO��ת����Ϊ60%
C. T2��ʱ������Ӧ��ƽ�������С�����������c(N2):c(NO)����
D. T1��ʱ������ʼʱ��Ӧ�������������һ�룬ƽ���NO��ת���ʼ�С