题目内容
【题目】(1)Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。
①该电池的负极材料是______________。电池工作时,电子流向______________(填“正极”或“负极”)。
②若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是______________。欲除去Cu2+,最好选用下列试剂中的______________(填字母序号)。
a.NaOH b.Zn c.Fe d.NH3·H2O
(2)给你提供纯锌片、纯铜片和500mL0.2mol·L-1的H2SO4溶液、导线、1000mL量筒。试用右图装置来测定锌和稀硫酸反应时在某段时间内通过导线的电子的物质的量。

①装置气密性良好,且1000mL量筒中已充满了水,则开始实验时,首先要______________。
②a电极材料为______________,其电极反应式为______________;b电极材料为______________,其电极反应式为______________。
③当量筒中收集672mL气体时(已折算成标准状况下),通过导线的电子的物质的量为_________。
【答案】 Zn(或锌) 正极 锌与Cu2+反应置换出Cu,构成铜锌原电池而加快了锌的腐蚀 b 用导线将a、b连接起来 锌(或Zn) Zn-2e-=Zn2+ 铜(或Cu) 2H++2e-=H2↑ 0.06mol
【解析】(1)①锌是活泼的金属,在反应中失去电子,因此该电池的负极材料是Zn。负极失去电子,所以电池工作时,电子流向正极。②由于锌与Cu2+反应置换出Cu,构成铜锌原电池而加快了锌的腐蚀,所以若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速锌电极的腐蚀。题目中a、c、d选项在除去铜离子的过程中都会引入杂质离子,应选Zn将Cu2+置换为单质而除去,答案选b;(2)①根据图示装置,要想求得电子转移的量,需要设计成锌、铜、硫酸原电池,量取金属锌和硫酸反应产生氢气的体积,根据原电池的构成条件,所以首先要用导线把a、b两电极连接起来;②锌、铜、硫酸原电池中,纯锌片是负极,电极反应:Zn-2e-=Zn2+;铜是正极,该极上电极反应为:2H++2e-=H2↑,所以a电极材料为锌,b电极材料为铜;(3)正极上电极反应为2H++2e-=H2↑,当量筒中收集到672mL即标况下0.03mol氢气时,转移电子是0.03mol×2=0.06mol。

【题目】一氧化碳、二氧化碳的利用具有十分重要的意义,科学家提出以下几个设想:
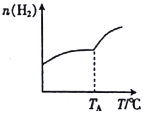
Ⅰ.二氧化碳与氢气在催化剂作用下可制取低碳烯烃。在一恒容密闭容器中分别投入1molCO2、3molH2,发生反应:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g) △H;在不同温度下,用传感技术测出平衡时H2的物质的量变化关系如图所示。
C2H4(g)+4H2O(g) △H;在不同温度下,用传感技术测出平衡时H2的物质的量变化关系如图所示。
(1)其他条件不变,起始时若按1molCO2、2molH2进行投料,则CO2的转化率将____________(填“增大”“ 减小”或“不变”)。
(2)△H____________ (填“>”“<”或“不能确定”)0。
(3)若测试中体系内无氧气产生,试结合图示推断热稳定性:C2H4_______(填“>” “<”或“不能确定”)H2O。
Ⅱ.甲醇是重要的化工原料,又可作为燃料,工业上可利用CO或CO2来生产燃料甲醇。已知制备甲醇的有关反应的化学方程式以及在不同温度下的化学平衡常数如下表所示。
化学反应 |
| 500 | 700 | 800 |
①2H2(g)+CO(g) | K1 | 2.5 | 0.34 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.0 | 1. 70 | 2.52 |
③3H2(g)+CO2 (g) | K3 |
请回答下列问题:
(4)根据反应比较△H1__________(填“>”“ <”或“不确定”)△H2。
(5)500℃时测得反应③在某时刻H2(g)、CO2
(6)下列措施能使反应③的平衡体系中![]() 增大的是___________(填字母)。
增大的是___________(填字母)。
A.将H2O(g)从体系中分离出去 B.充入He(g),使体系压强增大
C.升高温度 D.再充入1molH2
Ⅲ.(7)有人设想将CO按下列反应除去:2CO(g)=2C(s)+O2(g),请你分析该设想能否实现?_______________(填“能”或“不能”),依据是__________________。

