��Ŀ����
����Ŀ���ڲ�ͬ�¶��£���2L�ܱ������м���1mol NO��1mol����̿��������Ӧ��
2NO(g)+C(s) ![]() N2(g)+CO2(g) ��H=-213.5kJ/mol���ﵽƽ��ʱ���������£�
N2(g)+CO2(g) ��H=-213.5kJ/mol���ﵽƽ��ʱ���������£�
�¶�/�� | n(����̿)/mol | n(CO2)/mol |
T1 | X | |
T2 | 0.25 |
����˵������ȷ���ǣ� ��
A. T2��ʱ�����÷�Ӧ����10min�ﵽƽ�⣬��Ӧ����v(NO)=0.025mol/(L��min)
B. T1��ʱ�����÷�Ӧ��ƽ�ⳣ��K=9/16�����ƽ��ʱNO��ת����Ϊ60%
C. T2��ʱ������Ӧ��ƽ�������С�����������c(N2):c(NO)����
D. T1��ʱ������ʼʱ��Ӧ�������������һ�룬ƽ���NO��ת���ʼ�С
���𰸡�D
��������A. T2��ʱ�����÷�Ӧ����10min�ﵽƽ�⣬��CO2����0.25mol�����ݷ���ʽ��֪��NO����0.5mol������NO��ʾ�ķ�Ӧ����v��NO��=0.5mol��2L��10min=0.025mol/(Lmin)����A��ȷ��B. ��ﵽƽ��ʱNO����2ymol/L�����ݻ�ѧƽ������ʽ����ʽ���㣺
2NO(g)+C(s) ![]() N2(g)+CO2(g)
N2(g)+CO2(g)
��ʼŨ�ȣ�mol/L�� 0.5 0 0
ת��Ũ�ȣ�mol/L�� 2y y y
ƽ��Ũ�ȣ�mol/L��0.5��2y y y
��K=![]() =
= ![]() �����y=0.15����NO��ת����Ϊ��
�����y=0.15����NO��ת����Ϊ�� ![]() ��100%=60%����B��ȷ��C. ƽ�������С�����������ѹǿ������÷�Ӧǰ������������䣬����ƽ�ⲻ�ƶ�����c(N2):c(NO)���䣬��C��ȷ��D. T1��ʱ������ʼʱ��Ӧ�������������һ�룬�൱�ڼ�Сѹǿ����÷�Ӧǰ������������䣬ƽ�ⲻ�ƶ�����NO��ת���ʲ��䣬��D����ѡD��
��100%=60%����B��ȷ��C. ƽ�������С�����������ѹǿ������÷�Ӧǰ������������䣬����ƽ�ⲻ�ƶ�����c(N2):c(NO)���䣬��C��ȷ��D. T1��ʱ������ʼʱ��Ӧ�������������һ�룬�൱�ڼ�Сѹǿ����÷�Ӧǰ������������䣬ƽ�ⲻ�ƶ�����NO��ת���ʲ��䣬��D����ѡD��

 �Ķ��쳵ϵ�д�
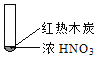
�Ķ��쳵ϵ�д�����Ŀ������ʵ���о��к���ɫ����������Աȷ������ý��۲���ȷ���ǣ�������
|
|
|
�� | �� | �� |
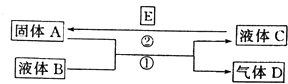
A. �����еĺ���ɫ���壬�ƶϲ���������һ���ǻ������
B. ����ɫ���岻�ܱ�������ľ̿��Ũ��������˷�Ӧ
C. ����˵��Ũ������лӷ��ԣ����ɵĺ���ɫ����Ϊ��ԭ����
D. ������������м���CO2���ɴ�˵��ľ̿һ����Ũ���ᷢ���˷�Ӧ