题目内容
6.化学实验有助于理解化学知识,形成化学观念.下列实验操作正确的是( )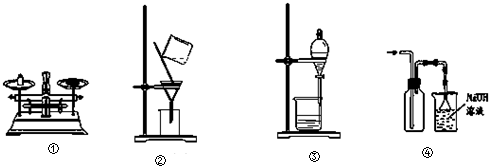
| A. | ①称量药品 | B. | ②过滤 | C. | ③分离乙醇和水 | D. | ④收集氯气 |
分析 A.称量时左物右码;
B.过滤液体时,要注意“一贴、二低、三靠”的原则;
C.乙醇和水互溶;
D.氯气能与氢氧化钠溶液反应.
解答 解:A.称量药品应左物右码和垫称量纸,不能直接在托盘上称量,故A错误;
B.漏斗下端应紧靠烧杯内壁,故B错误;
C.乙醇和水互溶,不能用分液分离,故C错误;
D.氯气能与氢氧化钠溶液反应,应使用防倒吸装置,故D正确.
故选D.
点评 本题考查化学实验基本操作,为高频考点,涉及气体收集、物质称量及分离与提纯等,侧重实验基本操作和实验原理的考查,注意装置的作用及实验的操作性、评价性分析,题目难度不大.

练习册系列答案
相关题目
16.25℃时,浓度均为0.2mol/L的NaHCO3和Na2CO3溶液中,下列判断不正确的是( )
| A. | 均存在电离平衡和水解平衡 | |
| B. | 分别加入NaOH固体,恢复至原温,c(CO32-)均增大 | |
| C. | c(OH-)前者大于后者 | |
| D. | 存在的粒子种类相同 |
17.用NA表示阿伏加德罗常数的数值.下列说法正确的是( )
| A. | 在O2参与的反应中,1 mol O2作氧化剂时得到的电子数一定是4NA | |
| B. | 1 L 1 mol•L-1 NH4NO3溶液中氮原子数小于2NA | |
| C. | 常温常压下,11.2 g乙烯中含有共用电子对数目为2.4NA | |
| D. | 标准状况下,22.4 L CHCl3中所含有的分子数为NA |
14.某物质的结构简式如图,关于该物质的下列说法中正确的是( )
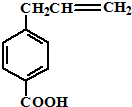

| A. | 该化合物的化学式为C10H11O2 | |
| B. | 分子中所有的碳原子不可能处于同一平面上 | |
| C. | 它的部分同分异构体能发生水解反应时则不能发生消去反应 | |
| D. | 该化合物能与新制的Cu(OH)2溶液发生反应生成砖红色沉淀且苯环上的一氯代物只有一种的同分异构体有4 |
1.下列物质的溶液在蒸发皿中加热蒸干并灼烧,可以得到该物质的是( )
| A. | FeSO4 | B. | MgSO4 | C. | AlCl3 | D. | NH4Cl |
11.选择正确答案的序号,填入下表空格中.
A、同位素 B、同分异构体 C、同系物 D、同素异形体 E、同一物质 F、同类物质
A、同位素 B、同分异构体 C、同系物 D、同素异形体 E、同一物质 F、同类物质
| 物质名称 | 相互关系 | 物质名称 | 相互关系 |
| ①氯仿与三氯甲烷 | ④氕、氘、氚 | ||
| ②一氯甲烷与四氯化碳 | ⑤白磷与红磷 | ||
| ③乙烷与新戊烷 | ⑥正丁烷与异丁烷 |
18.含有下列各组离子的溶液中,通入过量SO2气体后仍然能大量共存仍然能大量共存的是( )
| A. | H+、Na+、NH4+、NO3- | B. | K+、SO32-、Cl-、Na+ | ||
| C. | Ca2+、Cl-、Al3+、H+ | D. | Na+、I-、NH4+、HS- |
12.已知反应A2(g)+2B2(g)?2AB2(g)的△H<0,下列说法正确的是( )
| A. | 达到平衡后,增大压强有利于该反应平衡正向移动 | |
| B. | 达到化学平衡时,v正(A2)=2v逆(B2) | |
| C. | 升高温度,正向反应速率增加,逆向反应速率减小 | |
| D. | 达到平衡后,降低温度A2 气体的转化率减小 |
13.对于0.1mol•L-1 Na2CO3溶液,下列说法正确的是( )
| A. | 升高温度,溶液的pH降低 | |
| B. | c(Na+)=2c(CO32-)+c(HCO3-)+c(H2CO3) | |
| C. | c(Na+)+c(H+)=2 c(CO32-)+2c(HCO3-)+c(OH-) | |
| D. | 加入少量NaOH固体,c(CO32-)与c(Na+)均增大 |