题目内容
20.某溶液中有NH4+、Ca2+、Mg2+和Al3+四种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中浓度变化最大的离子是( )| A. | NH4+ | B. | Ca2+ | C. | Mg2+ | D. | Al3+ |
分析 加入过量的氢氧化钠溶液,微热并搅拌,四种离子均反应,铝离子转化为偏铝酸根离子,再加盐酸,又转化为铝离子,以此来解答.
解答 解:加入过量的氢氧化钠溶液,微热并搅拌,四种离子均反应:NH4+和OH-反应生成NH3逸出,导致后来物质的量变小;
Ca2+和NaOH以及后来加入的HCl不反应,故离子的物质的量不变;
Mg2+转化为Mg(OH)2沉淀后再与盐酸反应生成Mg2+,即后来Mg2+的物质的量不变;
Al3+转化为AlO2-,再加盐酸,又转化为Al3+,即后来Al3+的物质的量不变.
综上分析可知,浓度变化最大的是NH4+.
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.将pH=2的盐酸与pH=12的氨水等体积混合,在所得的混合溶液中,下列关系式正确的是( )
| A. | c(Cl-)>c(NH4+)>c(OH-)>c(H+) | B. | c(NH4+)>c(Cl-)>c(OH-)>c(H+) | ||
| C. | c(Cl-)=c(NH4+)>c(H+)=c(OH-) | D. | c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
11.下列说法正确的是( )
| A. | HCHO溶液、(NH4)2SO4溶液均能使蛋白质变性 | |
| B. | 分子式为C2H4O2的有机物不一定是羧酸 | |
| C. | 煤的干馏是物理变化,煤的气化和液化是化学变化 | |
| D. | 纤维素、蛋白质、油脂、糖类在一定条件下都能发生水解反应 |
8.链状单炔烃完全燃烧后生成的二氧化碳与水的物质的量之比为5:4,满足上述条件的烃的种数共有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
5.a、b、c、d是原子序数依次递增的四种元素,a、b、c三种元素的原子核外电子数之和与Cl-的核外电子数相等,a、c分别得到一个电子后均形成稀有气体原子的稳定电子层结构,d是生活中用量最大的金属,其简单离子有两种常见价态,下列说法正确的是( )
| A. | 离子半径:c>b>a | |
| B. | a与c形成化合物的溶液有毒,要密封保存于玻璃瓶中 | |
| C. | a2b2与d的一种较高价态离子的盐溶液混合时会产生大量的b2 | |
| D. | d高价离子在溶液中与c的低价离子因发生氧化还原反应而不能大量共存 |
12.对于化学反应中的能量变化,表述正确的是( )
| A. | 氧化还原反应均为放热反应 | B. | 放热反应中,反应后体系能量降低 | ||
| C. | 断开化学键的过程会放出能量 | D. | 加热才能发生的反应均为吸热反应 |
9.有机物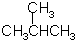 的名称是( )
的名称是( )
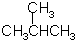 的名称是( )
的名称是( )| A. | 2-甲基丁烷 | B. | 2-甲基丙烷 | C. | 1,1-二甲基乙烷 | D. | 三甲基甲烷 |

 .
. .
.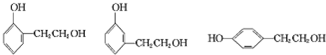 .
.