题目内容
8.链状单炔烃完全燃烧后生成的二氧化碳与水的物质的量之比为5:4,满足上述条件的烃的种数共有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
分析 设链状单炔烃的分子式为CnH2n-2,则生成的二氧化碳与水的物质的量之比n:(n-1)=5:4,解得n=5,根据碳链异构和位置异构写出满足条件的同分异构体.
解答 解:设链状单炔烃的分子式为CnH2n-2,则生成的二氧化碳与水的物质的量之比n:(n-1)=5:4,解得n=5,即此单炔烃为C5H8.
根据碳链异构和位置异构可知,满足条件的炔烃为:CH≡CCH2CH2CH3,CH3C≡CCH2CH3,(CH3)2CHC≡CH,故选A.
点评 本题考查了同分异构体的书写,难度不大,根据碳链异构和位置异构来分析.

练习册系列答案
 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
18.如表为元素周期表中的一部分,列出11种元素在元素周期表中的位置.用化学符号回答下列各问题.
(1)11种元素中,第一电离能最小的是K;电负性最大的是F.(都用化学符号表示)
(2)④、⑤、⑥三种元素最高价氧化物对应的水化物中,呈两性的是Al(OH)3.(填化学式)
(3)元素②的氢化物的电子式为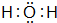 ;该氢化物常温下和元素④的单质反应的化学方程式为2Na+2H2O=2NaOH+H2↑
;该氢化物常温下和元素④的单质反应的化学方程式为2Na+2H2O=2NaOH+H2↑
(4)④和⑦的最高价氧化物对应水化物的化学式分别为NaOH和HClO4.④和(11)两元素形成化合物的化学式为NaBr; 该化合物灼烧时的焰色为黄色
(5)第一电离能:⑤>⑥(填“>”“<”“=”),请说明原因:Mg元素原子3s能级容纳2个电子,为全满稳定状态,能量较低.
| 主族 周期 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | VII | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ | (11) |
(2)④、⑤、⑥三种元素最高价氧化物对应的水化物中,呈两性的是Al(OH)3.(填化学式)
(3)元素②的氢化物的电子式为
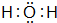 ;该氢化物常温下和元素④的单质反应的化学方程式为2Na+2H2O=2NaOH+H2↑
;该氢化物常温下和元素④的单质反应的化学方程式为2Na+2H2O=2NaOH+H2↑(4)④和⑦的最高价氧化物对应水化物的化学式分别为NaOH和HClO4.④和(11)两元素形成化合物的化学式为NaBr; 该化合物灼烧时的焰色为黄色
(5)第一电离能:⑤>⑥(填“>”“<”“=”),请说明原因:Mg元素原子3s能级容纳2个电子,为全满稳定状态,能量较低.
19.下列反应的离子方程式正确的是( )
| A. | 氯气通入氢氧化钠溶液中 Cl2+2OH-=Cl-+ClO-+H2O | |
| B. | 金属铁与稀硝酸反应 Fe+2H+=Fe2++H2↑ | |
| C. | 在硅酸钠溶液中滴加稀硫酸 SiO32-+2H+=H2SO3↓ | |
| D. | 铜粉与98.3%的硫酸加热下反应 Cu+4H++SO42-=Cu2++SO2↑+2H2O |
16.某同学用如图所示装置制备并检验Cl2的性质.下列说法正确的是( )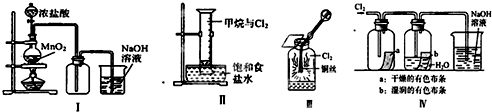

| A. | Ⅰ图中:如果MnO2过量,浓盐酸就可全部被消耗 | |
| B. | Ⅱ图中:量筒中发生了加成反应 | |
| C. | Ⅲ图中:生成蓝色的烟 | |
| D. | Ⅳ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成 |
3.某同学想用实验证明高锰酸钾溶液的紫红色是MnO4-离子的颜色,而不是K+离子的颜色,他设计的下列实验步骤中没有意义的是( )
| A. | 将高锰酸钾晶体加热分解,所得固体质量减少 | |
| B. | 观察氯化钾溶液没有颜色,表明溶液中K+无色 | |
| C. | 在氯化钾溶液中加入适量锌粉振荡,静置后未见明显变化,表明锌与K+无反应 | |
| D. | 在高锰酸钾溶液中加入适量锌粉振荡,静置后见紫红色褪去,表明MnO4-离子为紫红色 |
20.某溶液中有NH4+、Ca2+、Mg2+和Al3+四种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中浓度变化最大的离子是( )
| A. | NH4+ | B. | Ca2+ | C. | Mg2+ | D. | Al3+ |
17. 下表为周期表中短周期的一部分.已知a原子的最外层电子数是电子总数的三分之一,下列说法中正确的是( )
下表为周期表中短周期的一部分.已知a原子的最外层电子数是电子总数的三分之一,下列说法中正确的是( )
 下表为周期表中短周期的一部分.已知a原子的最外层电子数是电子总数的三分之一,下列说法中正确的是( )
下表为周期表中短周期的一部分.已知a原子的最外层电子数是电子总数的三分之一,下列说法中正确的是( )| A. | a的最高价氧化物对应水化物有两性 | |
| B. | b与d组成的化合物不能与水反应 | |
| C. | c的单质能与强碱反应生成两种盐 | |
| D. | c与d能形成共价化合物和离子化合物 |
18.下列物质中,化学键类型(离子键、共价键)完全相同的是( )
| A. | HI和NaI | B. | NaF和NaOH | C. | Na2SO4和KNO3 | D. | F2和NaCl |
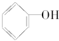 B.
B.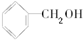 C.甲醇 D.CH3-O-CH3E.HO-CH2CH2-OH
C.甲醇 D.CH3-O-CH3E.HO-CH2CH2-OH