题目内容
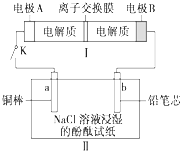 如图所示装置Ⅰ是一种可充电电池,装置Ⅱ为电解池.离子交换膜只允许Na+通过,充放电的化学方程式为Na2S4+3NaBr
如图所示装置Ⅰ是一种可充电电池,装置Ⅱ为电解池.离子交换膜只允许Na+通过,充放电的化学方程式为Na2S4+3NaBr
| ||
| 放电 |
| A、负极反应为4Na-4e-═4Na+ |
| B、闭合K后,b电极附近的pH变小 |
| C、闭合K后,a电极上有气体产生 |
| D、当有0.01mol Na+通过离子交换膜时,b电极上析出标准状况下的气体112mL |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:闭合开关K时,II为电解池、I为原电池,b极附近先变红色,则b为阴极、a为阳极,A为原电池正极、B为原电池负极,负极反应为2Na2S2-2e-=2Na++Na2S4,正极反应为NaBr3+2Na++2e-=3NaBr,a电极反应为2H++2e-=H2↑、阳极反应为 2Cu-2e-=Cu2+,据此解答.
解答:
解:A.负极反应为2Na2S2-2e-=2Na++Na2S4,故A错误;
B.闭合K后,b电极氢离子放电导致氢氧根离子浓度增大,所以b电极附近的pH增大,故B错误;
C.闭合K后,a电极上电极反应为2Cu-2e-=Cu2+,所以没有气体生成,故C错误;
D.闭合K时,有0.01molNa+通过离子交换膜,说明有0.01mol电子转移,阴极上生成0.005molH2,标准状况下体积为0.005mol×22.4L/mol=0.112L=112mL,故D正确;
故选D.
B.闭合K后,b电极氢离子放电导致氢氧根离子浓度增大,所以b电极附近的pH增大,故B错误;
C.闭合K后,a电极上电极反应为2Cu-2e-=Cu2+,所以没有气体生成,故C错误;
D.闭合K时,有0.01molNa+通过离子交换膜,说明有0.01mol电子转移,阴极上生成0.005molH2,标准状况下体积为0.005mol×22.4L/mol=0.112L=112mL,故D正确;
故选D.
点评:本题考查了原电池和电解池原理,为高考热点,根据b电极溶液颜色变化确定正负极、阴阳极,注意正负极上电极反应式的书写,为难点.

练习册系列答案
相关题目
下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A、常温常压下,28g N2所含有的原子数目为2NA |
| B、42g C2H4和C3H6的混合物中原子数为3NA |
| C、12g金刚石中的C-C键数目为4NA个 |
| D、标准状况下,NA个H2O占有的体积为22.4L |
下列离子方程式中,不正确的是( )
| A、偏铝酸钠溶液中通入适量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
| B、向FeCl3溶液中滴加几滴KSCN溶液:Fe3++SCN-═[Fe(SCN)]2+ |
| C、NaHCO3与足量石灰水反应:2HCO3-+Ca2++2OH-═2H2O+CaCO3↓+CO32- |
| D、偏铝酸钠溶液中加过量盐酸:AlO2-+4H+═Al3++2H2O |
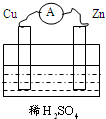 如图将Cu、Zn两种金属片插入稀H2SO4中,构成铜锌原电池,下列关于铜锌原电池的叙述正确的是( )
如图将Cu、Zn两种金属片插入稀H2SO4中,构成铜锌原电池,下列关于铜锌原电池的叙述正确的是( )| A、溶液中的H+向负极移动 |
| B、Zn片作负极,发生还原反应 |
| C、溶液的PH值将增大 |
| D、电子从Cu流出经导线流向Zn |
下列各组物质互为同系物的是( )
| A、金刚石和石墨 |
| B、正丁烷和异丁烷 |
| C、甲烷和乙烷 |
| D、白磷和红磷 |
下列有关电解质溶液的说法正确的是( )
| A、将pH=2的NH4Cl与pH=12氨水等体积混合,溶液中:c(NH4+)=c(Cl-) | ||||
| B、溶液中c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) | ||||
| C、1.0mol?L-1的H2SO4溶液80℃时的pH大于25℃时pH | ||||
D、对氨水进行稀释,
|
甲基环己烷可由甲苯与氢气加成制得,其环上一氯代物的同分异构体数目是( )
| A、4 | B、3 | C、2 | D、1 |
在由水电离出的c(H+)=1×10-13mol/L的溶液中,一定可以大量共存的是( )
| A、Ba2+Na+ NO3-Cl- |
| B、Fe2+ Na+ NO3- Cl- |
| C、SO42-SO32- NH4+Na+ |
| D、Mg2+Na+Br-AlO2- |