题目内容
某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量)( )


| A、反应Ⅰ:△H>0,P2>P1 |
| B、反应Ⅱ:△H>0,T1>T2 |
| C、反应Ⅲ:△H>0,T2>T1;或△H<0,T2<T1 |
| D、反应Ⅳ:△H<0,T2>T1 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:反应Ⅰ说明升高温度,A的转化率降低,增大压强平衡向正反应方向移动;
反应Ⅱ由图象可以看出T1>T2,升高温度C的物质的量减少;
反应Ⅲ中温度的高低与温度对平衡移动的影响有关;
反应Ⅳ,由图象可以看出T2条件下A的转化率大,因此当T2>T1时,说明升高温度平衡向正反应方向进行,正反应为吸热反应△H>0,反应为放热反应.
反应Ⅱ由图象可以看出T1>T2,升高温度C的物质的量减少;
反应Ⅲ中温度的高低与温度对平衡移动的影响有关;
反应Ⅳ,由图象可以看出T2条件下A的转化率大,因此当T2>T1时,说明升高温度平衡向正反应方向进行,正反应为吸热反应△H>0,反应为放热反应.
解答:
解:A.反应Ⅰ的特点是正反应方向为气体体积减小的方向,结合图象,压强增大A的转化率应增大,所以p2>p1,它随温度的升高A的转化率降低,所以正反应为放热反应△H<0,故A错误.
B.关于反应Ⅱ由图象可以看出T1条件下达到平衡所用的时间少,所以T1>T2,而在T1条件下达平衡时n(C)小,所以说明低温有利于C的生成,故它主要的正反应为放热反应△H<0,B错误;
C.关于反应Ⅲ,由图象可以看出,T2条件下C的平衡体积分数大,因此当T2>T1时正反应为吸热反应△H>0,而当T2<T1时正反应为放热反应△H<0,故C正确;
D.关于反应Ⅳ,由图象可以看出T2条件下A的转化率大,因此当T2>T1时,说明升高温度平衡向正反应方向进行,因此正反应为吸热反应△H>0,故D错误.
故选C.
B.关于反应Ⅱ由图象可以看出T1条件下达到平衡所用的时间少,所以T1>T2,而在T1条件下达平衡时n(C)小,所以说明低温有利于C的生成,故它主要的正反应为放热反应△H<0,B错误;
C.关于反应Ⅲ,由图象可以看出,T2条件下C的平衡体积分数大,因此当T2>T1时正反应为吸热反应△H>0,而当T2<T1时正反应为放热反应△H<0,故C正确;
D.关于反应Ⅳ,由图象可以看出T2条件下A的转化率大,因此当T2>T1时,说明升高温度平衡向正反应方向进行,因此正反应为吸热反应△H>0,故D错误.
故选C.
点评:本题考查外界条件对化学平衡的影响,题目难度中等,本题注意分析图象中曲线的变化趋势,结合方程式的特征以及外界条件对平衡移动的影响分析.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法正确的是( )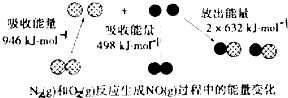
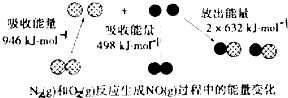
| A、通常情况下,N2(g)和O2(g)混合能直接生成NO |
| B、1mol N2(g)和NA个O2(g)反应放出的能量为180kJ |
| C、NO是一种酸性氧化,能与NaOH溶液反应生成盐和水 |
| D、1mol N2(g)和1mol O2(g)具有的总能量小于2mol NO(g)具有的总能量 |
9g二氧化碳和一氧化碳组成的混合气体与一定量O2恰好完全反应后得到二氧化碳5.6L(标准状况),下列说法正确的是( )
| A、反应前CO和CO2的体积比为1:1 |
| B、反应前CO和CO2的质量比为1:1 |
| C、反应前CO和CO2的混合气体与反应后气体体积比(同温同压下)为1:2 |
| D、反应前CO和CO2的混合气体与反应后气体所含氧原子的个数比为1:2 |
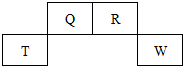 短周期元素Q、R、T、W在元素周期表中的位置如图,其中T所处的周期序数与主族序数相等,下列叙述正确的是( )
短周期元素Q、R、T、W在元素周期表中的位置如图,其中T所处的周期序数与主族序数相等,下列叙述正确的是( )| A、离子半径:Tm+>Wn- |
| B、非金属性:Q<W |
| C、R的氢化物的水溶液呈酸性 |
| D、Q的氧化物都是酸性氧化物 |
将氯化钠、氯化铝、氯化亚铁、氯化铁、氯化镁五种溶液,只用一种试剂并通过一步实验就能加以区别.这种试剂是( )
| A、AgNO3 |
| B、NaOH |
| C、H2SO4 |
| D、BaCl2 |
下列物质性质的变化规律中与共价键键能大小有关的是( )
①F2、Cl2、Br2、I2的熔点、沸点逐渐升高;②HF、HCl、HBr、HI的热稳定性依次减弱
③金刚石的硬度、熔点、沸点都高于晶体硅;④NaF、NaCl、NaBr、NaI熔点依次降低.
①F2、Cl2、Br2、I2的熔点、沸点逐渐升高;②HF、HCl、HBr、HI的热稳定性依次减弱
③金刚石的硬度、熔点、沸点都高于晶体硅;④NaF、NaCl、NaBr、NaI熔点依次降低.
| A、仅③ | B、①③ | C、②④ | D、②③ |
下列与实验相关的叙述正确的是( )
| A、测定中和热时,应将NaOH溶液分次缓慢倒入装有盐酸的烧杯中,并搅拌 |
| B、配置溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 |
| C、酸碱滴定时,若加入待测前用待测液润洗锥形瓶,将导致测定结果偏高 |
| D、检验某溶液是否含有SO42-时,应取少量溶液,依次加入BaCl2溶液和稀盐酸 |
常温下,0.01mol?L-1 MOH溶液的pH为10.已知:
2MOH(aq)+H2SO4(aq)═M2SO4(aq)+2H2O(l)△H1=-24.2kJ?mol-1;
H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ?mol-1
则MOH在水溶液中电离的△H为( )
2MOH(aq)+H2SO4(aq)═M2SO4(aq)+2H2O(l)△H1=-24.2kJ?mol-1;
H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ?mol-1
则MOH在水溶液中电离的△H为( )
| A、+33.1kJ?mol-1 |
| B、+45.2kJ?mol-1 |
| C、-81.5kJ?mol-1 |
| D、-33.1kJ?mol-1 |
将0.5mol Na投入过量的水(m1g)中,得到a g溶液;将0.5mol Zn投入过量的盐酸(m2g)中,得到bg溶液,若m1═m2,则a.b的质量关系是( )
| A、a>b | B、a<b |
| C、a=b | D、不能确定 |