题目内容
将0.5mol Na投入过量的水(m1g)中,得到a g溶液;将0.5mol Zn投入过量的盐酸(m2g)中,得到bg溶液,若m1═m2,则a.b的质量关系是( )
| A、a>b | B、a<b |
| C、a=b | D、不能确定 |
考点:化学方程式的有关计算
专题:计算题
分析:反应的方程式分别为:2Na+2H2O=2NaOH+H2↑,Mg+2HCl=MgCl2+H2↑,根据方程式计算生成氢气的质量,进而表示出反应后溶液的质量,据此判断.
解答:
解:由2Na+2H2O=2NaOH+H2↑,可知0.5mol钠反应生成氢气为:0.5mol×
=0.25mol,则生成m(H2)=0.25mol×2g/mol=0.5g,m(Na)=0.5mol×23g/mol=11.5g,反应后溶液的质量为:m1+(11.5-0.5)g=(m1+11)g=ag,
由Mg+2HCl=MgCl2+H2↑,可知0.5molMg反应生成0.5mol氢气,则m(H2)=0.5mol×2g/mol=1g,m(Mg)=0.5mol×24g/mol=12g,反应后溶液的质量为:m2+(12-1)g=(m2+11)g=bg,
若m1=m2,则a和b的质量关系相等,
故选C.
| 1 |
| 2 |
由Mg+2HCl=MgCl2+H2↑,可知0.5molMg反应生成0.5mol氢气,则m(H2)=0.5mol×2g/mol=1g,m(Mg)=0.5mol×24g/mol=12g,反应后溶液的质量为:m2+(12-1)g=(m2+11)g=bg,
若m1=m2,则a和b的质量关系相等,
故选C.
点评:本题考查化学方程式的计算,侧重于学生的分析能力和计算能力的考查,注意把握相关方程式的书写,根据方程式计算即可,难度不大.

练习册系列答案
相关题目
某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量)( )


| A、反应Ⅰ:△H>0,P2>P1 |
| B、反应Ⅱ:△H>0,T1>T2 |
| C、反应Ⅲ:△H>0,T2>T1;或△H<0,T2<T1 |
| D、反应Ⅳ:△H<0,T2>T1 |
有人建议将氢元素排在元素周期表的ⅦA族.下列事实能支持这一观点的是( )
①H原子得到一个电子实现最外电子层稳定结构;
②氢分子的结构式为H-H;
③与碱金属元素形成离子化合物:M+[:H]-
④分子中原子间的化学键都属于非极性键.
①H原子得到一个电子实现最外电子层稳定结构;
②氢分子的结构式为H-H;
③与碱金属元素形成离子化合物:M+[:H]-
④分子中原子间的化学键都属于非极性键.
| A、①②③ | B、①③④ |
| C、②③④ | D、①②③④ |
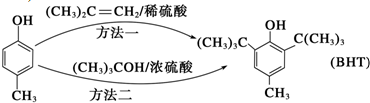
近年来,食品安全事故频繁发生,人们对食品添加剂的认识逐渐加深.Butylated Hydroxy Toluene(简称BHT)是一种常用的食品抗氧化剂,合成方法有如下两种:下列说法正确的是( )

A、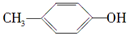 能与Na2CO3溶液反应生成CO2 能与Na2CO3溶液反应生成CO2 |
| B、BHT久置于空气中不会被氧化 |
| C、两种方法的反应类型都是加成反应 |
D、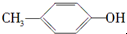 与BHT互为同系物 与BHT互为同系物 |
短周期元素X,Y,Z在周期表中的位置如图所示,则下列说法中错误的是( )
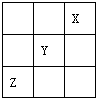

| A、X、Y、Z中X的单质最稳定 |
| B、Y的氢化物为HY |
| C、Z的最高价氧化物的化学式为ZO2 |
| D、能发生Cl2+H2Z═Z+2HCl的反应 |
下列说法正确的是( )
| A、发生化学反应时失去电子越多的金属原子,还原能力越强 |
| B、金属阳离子被还原后,不一定得到该元素的单质 |
| C、核外电子总数相同的粒子,一定是同种元素的原子 |
| D、只能与酸反应的氧化物,一定是碱性氧化物 |
下列各组微粒中,氧化性依次增强,且半径依次减小的是( )
| A、O、Cl、S、P |
| B、K+、Mg2+、Al3+、H+ |
| C、I-、Br-、Cl-、S2- |
| D、Al3+、Mg2+、Ca2+、Ba2+ |
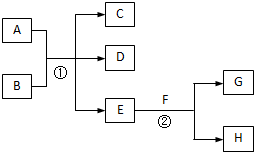 在下列各变化中,E为无色无味的液体(常温下),F为淡黄色粉末,G为常见的无色气体(反应条件均已省略).
在下列各变化中,E为无色无味的液体(常温下),F为淡黄色粉末,G为常见的无色气体(反应条件均已省略).