题目内容
将氯化钠、氯化铝、氯化亚铁、氯化铁、氯化镁五种溶液,只用一种试剂并通过一步实验就能加以区别.这种试剂是( )
| A、AgNO3 |
| B、NaOH |
| C、H2SO4 |
| D、BaCl2 |
考点:物质的检验和鉴别的实验方案设计
专题:物质检验鉴别题
分析:都为氯化物,可根据阳离子的不同选择检验方法,可加入碱,生成沉淀的颜色、现象不同.
解答:
解:A.均与硝酸银反应生成AgCl白色沉淀,现象相同,不能鉴别,故A不选;
B.分别滴加NaOH溶液时,产生白色沉淀的是氯化镁;先产生沉淀,后沉淀溶解的是氯化铝;产生红褐色沉淀的是氯化铁;产生白色沉淀,后又变灰绿色,最后变成红褐色的是氯化亚铁;无现象的是氯化钠,现象不同,可鉴别,故B选;
C.均不与硫酸反应,不能鉴别,故C不选;
D.均不与氯化钡反应,不能鉴别,故D不选;
故选B.
B.分别滴加NaOH溶液时,产生白色沉淀的是氯化镁;先产生沉淀,后沉淀溶解的是氯化铝;产生红褐色沉淀的是氯化铁;产生白色沉淀,后又变灰绿色,最后变成红褐色的是氯化亚铁;无现象的是氯化钠,现象不同,可鉴别,故B选;
C.均不与硫酸反应,不能鉴别,故C不选;
D.均不与氯化钡反应,不能鉴别,故D不选;
故选B.
点评:本题考查物质的检验和鉴别的实验方案的设计,题目难度不大,本题注意根据金属阳离子的性质不同选择检验试剂,注意碱的颜色和水溶性.

练习册系列答案
相关题目
短周期元素X、Y、Z在元素周期表中的位置如图所示,下列说法正确的是( )
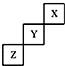

| A、X、Y、Z三种元素中,单质在常温下均为气态 |
| B、Z的氢化物的稳定性比Y的强 |
| C、Y的最高正化合价为+5 |
| D、Y的单质的熔点比Z的低 |
下列化学反应的离子方程式其中正确的是( )
| A、铁与氯化铁溶液反应:Fe+2Fe3+═3Fe2+ |
| B、氨水与盐酸反应:OH-+H+═H2O |
| C、氢氧化钡溶液与硫酸反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| D、碳酸钙与盐酸反应:CO32-+2H+═CO2↑+H2O |
三氟化氮(NF3)(提示氟只有两种价态:-1,0)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3NF3+5H2O=2NO+HNO3+9HF.下列有关该反应的说法正确的是( )
| A、NF3是氧化剂,H2O是还原剂 |
| B、还原剂与氧化剂的物质的量之比为2:1 |
| C、若生成0.2mol HNO3,则转移0.2mol电子 |
| D、若1molNF3被氧化反应转移电子数为2NA |
下列各组离子中,在指定溶液中一定能大量存在的是( )
| A、澄清透明的无色溶液:ClO-、MnO4-、Al3+、SO42- |
| B、含有大量Fe3+的溶液:H+、I-、K+、Cl- |
| C、能使pH试纸变深蓝色的溶液:Na+、AlO2-、S2-、CO32- |
| D、由水电离产生的c(H+)=1×10-12mol/L的溶液:NH4+、Na+、Cl-、HCO3- |
某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量)( )


| A、反应Ⅰ:△H>0,P2>P1 |
| B、反应Ⅱ:△H>0,T1>T2 |
| C、反应Ⅲ:△H>0,T2>T1;或△H<0,T2<T1 |
| D、反应Ⅳ:△H<0,T2>T1 |
用NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、1.0L 1.0mol?L-1 CH3COOH溶液中,CH3COOH分子数为NA |
| B、1mol Na2O2与足量H2O反应转移的电子数NA |
| C、常温常压下,22.4L氧气含有氧原子为2NA |
| D、1.8g重水(D2O)中,含有的质子数为0.1NA |
工业上合成甲醇一般采用下列反应:CO(g)+2H(g)?CH30H(g)△H<0,下表是该反应在不同温度下的化学平衡常数(K):
则下列数据符合表中x的是( )
| 温度/℃ | 250 | 350 |
| K/(mol?L-2)-2 | 2.041 | x |
| A、0 | B、0.012 |
| C、32.081 | D、100 |
短周期元素X,Y,Z在周期表中的位置如图所示,则下列说法中错误的是( )
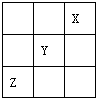

| A、X、Y、Z中X的单质最稳定 |
| B、Y的氢化物为HY |
| C、Z的最高价氧化物的化学式为ZO2 |
| D、能发生Cl2+H2Z═Z+2HCl的反应 |