题目内容
常温下,0.01mol?L-1 MOH溶液的pH为10.已知:
2MOH(aq)+H2SO4(aq)═M2SO4(aq)+2H2O(l)△H1=-24.2kJ?mol-1;
H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ?mol-1
则MOH在水溶液中电离的△H为( )
2MOH(aq)+H2SO4(aq)═M2SO4(aq)+2H2O(l)△H1=-24.2kJ?mol-1;
H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ?mol-1
则MOH在水溶液中电离的△H为( )
| A、+33.1kJ?mol-1 |
| B、+45.2kJ?mol-1 |
| C、-81.5kJ?mol-1 |
| D、-33.1kJ?mol-1 |
考点:有关反应热的计算
专题:化学反应中的能量变化
分析:由题意知MOH是弱碱:MOH(aq)+H+(aq)═M+(aq)+H2O(l)△H1=-12.1 kJ?mol-1①,H+(aq)+OH-(aq)═H2O(l)△H2=-57.3 kJ?mol-1②,根据盖斯定律构造方程式MOH(aq)??M+(aq)+OH-(aq)并计算焓变.
解答:
解:常温下,0.01mol?L-1 MOH溶液的pH为10,说明MOH是弱碱:MOH(aq)+H+(aq)═M+(aq)+H2O(l)△H1=-12.1 kJ?mol-1①,
H+(aq)+OH-(aq)═H2O(l)△H2=-57.3 kJ?mol-1②,
根据盖斯定律,由①-②得:MOH(aq)??M+(aq)+OH-(aq)△H=(-12.1+57.3)kJ?mol-1=+45.2 kJ?mol-1,
故选B.
H+(aq)+OH-(aq)═H2O(l)△H2=-57.3 kJ?mol-1②,
根据盖斯定律,由①-②得:MOH(aq)??M+(aq)+OH-(aq)△H=(-12.1+57.3)kJ?mol-1=+45.2 kJ?mol-1,
故选B.
点评:本题考查了弱电解质的判断和反应热的计算,综合性较强,注意弱电解质的判断和利用盖斯定律进行构造目标热化学方程式并计算焓变是解题的关键.

练习册系列答案
相关题目
下列反应的离子方程式书写正确的是( )
A、等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:Ba2++2OH-+2HCO
| ||
| B、氢氧化铁溶于氢碘酸溶液:Fe(OH)3+3H+═Fe3++3H2O | ||
C、向亚硫酸钠溶液中加入足量硝酸:SO
| ||
| D、铜溶解于氯化铁溶液中:2Fe3++Cu═2Fe2++Cu2+ |
某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量)( )


| A、反应Ⅰ:△H>0,P2>P1 |
| B、反应Ⅱ:△H>0,T1>T2 |
| C、反应Ⅲ:△H>0,T2>T1;或△H<0,T2<T1 |
| D、反应Ⅳ:△H<0,T2>T1 |
分子式为C5H8的有机物,其结构不可能的是( )
| A、只含有一个双键的链状有机物 |
| B、含有两个双键的链状有机物 |
| C、含有两个双键的环状有机物 |
| D、含有一个叁键的链状有机物 |
工业上合成甲醇一般采用下列反应:CO(g)+2H(g)?CH30H(g)△H<0,下表是该反应在不同温度下的化学平衡常数(K):
则下列数据符合表中x的是( )
| 温度/℃ | 250 | 350 |
| K/(mol?L-2)-2 | 2.041 | x |
| A、0 | B、0.012 |
| C、32.081 | D、100 |
CH4中混有C2H4,欲除去C2H4得到纯净的CH4,最好依次通过盛有下列哪一组试剂的洗气瓶( )
| A、澄清石灰水,浓H2SO4 |
| B、酸性KMnO4溶液,浓H2SO4 |
| C、Br2水,浓H2SO4 |
| D、浓H2SO4,酸性KMnO4溶液 |
有人建议将氢元素排在元素周期表的ⅦA族.下列事实能支持这一观点的是( )
①H原子得到一个电子实现最外电子层稳定结构;
②氢分子的结构式为H-H;
③与碱金属元素形成离子化合物:M+[:H]-
④分子中原子间的化学键都属于非极性键.
①H原子得到一个电子实现最外电子层稳定结构;
②氢分子的结构式为H-H;
③与碱金属元素形成离子化合物:M+[:H]-
④分子中原子间的化学键都属于非极性键.
| A、①②③ | B、①③④ |
| C、②③④ | D、①②③④ |
近年来,食品安全事故频繁发生,人们对食品添加剂的认识逐渐加深.Butylated Hydroxy Toluene(简称BHT)是一种常用的食品抗氧化剂,合成方法有如下两种:下列说法正确的是( )
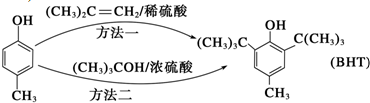

A、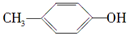 能与Na2CO3溶液反应生成CO2 能与Na2CO3溶液反应生成CO2 |
| B、BHT久置于空气中不会被氧化 |
| C、两种方法的反应类型都是加成反应 |
D、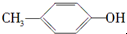 与BHT互为同系物 与BHT互为同系物 |