题目内容
14.某酸式盐NaHY的水溶液显碱性,下列叙述不正确的是( )| A. | H2Y的电离方程式:H2Y?2H++Y2- | |
| B. | HY- 离子水解的离子方程式:HY-+H2O?H2Y+OH- | |
| C. | 该酸式盐溶液中离子浓度大小关系:c(Na+)>c(HY-)>c(OH-)>c(H+) | |
| D. | 该酸式盐溶液中离子浓度关系:c(H+)+c(H2Y)═c(OH-)+c(Y2-) |
分析 A、H2Y是二元弱酸,电离时分两步电离;
B、HY-离子水解生成H2Y;
C、某酸的酸式盐NaHY的水溶液显碱性,HY-的电离程度小于HY-的水解程度,据此判断各种离子浓度大小;
D、根据溶液电荷守恒和物料守恒的角度分析.
解答 解:A、H2Y是二元弱酸,电离时分两步电离,第一步电离生成氢离子和酸式酸根离子,电离方程式为:H2Y+H2O?HY-+H3O+,故A错误;
B、HY-离子水解生成H2Y,所以HY-离子水解的离子方程式:HY-+H2O?H2Y+OH-,故B正确;
C、某酸的酸式盐NaHY的水溶液中,阴离子水解,钠离子不水解,所以c(Na+)>c(HY-),HY-的电离程度小于水解程度,但无论电离还是水解都较弱,阴离子还是以HY-为主,溶液呈碱性,说明溶液中c(OH-)>c(H+),所以离子浓度大小顺序为c(Na+)>c(HY-)>c(OH-)>c(H+),故C正确;
D、溶液中存在电荷守恒:c(H+)+c(Na+)=c(HY-)+2c(Y2-)+c(OH-),物料守恒:c(Na+)=c(HY-)+c(Y2-)+c(H2Y),二者联式可得c(H+)+c(H2Y)=c(OH-)+c(Y2-),故D正确;
故选A.
点评 本题考查了多元弱酸的电离,弱酸盐的水解,离子浓度的大小比较,题目难度中等,本题易错点为D,注意从溶液的电荷守恒和物料守恒的角度分析.

练习册系列答案
 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
2.某校化学小组学生利用如图所示装置进行“乙二酸(俗名草酸)晶体受热分解”的实验,并验证分解产物中有CO2和CO.(图中夹持装置及尾气处理装置均已略去)
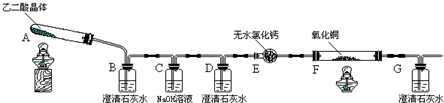
(1)装置C中盛放NaOH溶液的作用是吸收乙二酸晶体受热分解生成的二氧化碳
(2)①证明分解产物中有CO2的现象是装置B中澄清石灰水变浑浊
②证明分解产物中有CO的现象是装置D中澄清石灰水不变浑浊,装置F中黑色氧化铜变为红色固体,装置G中澄清石灰水变浑浊
(3)实验结束后,装置F中黑色氧化铜变为红色固体.简述检验红色固体中是否含有Cu2O的实验方法(已知Cu2O溶于稀硫酸生成铜单质和硫酸铜):取少量固体与试管中,加稀硫酸,若溶液变蓝色,说明有Cu2O,若溶液不变色,则不含有Cu2O
(4)①草酸和草酸钠(Na2C2O4)可以在酸性条件下被KMnO4、MnO2氧化.KMnO4和草酸钠在稀硫酸中反应的离子方程式是2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O.
②实验室常用草酸钠标定KMnO4溶液.操作如下:准确称取0.2000g草酸钠,放入锥形瓶中,加100mL稀硫酸溶解,用配置好的KMnO4溶液滴定.当加入1滴KMnO4溶液后,锥形瓶中溶液立即由无色变为紫红色,且30s不褪色,即达到滴定终点.重复上述滴定操作三次,实验数据如下表所示.
KMnO4溶液的物质的量浓度的计算式是c(KMnO4)=$\frac{0.2000g×2mol}{5mol×134g/mol×0.01601L}$.

(1)装置C中盛放NaOH溶液的作用是吸收乙二酸晶体受热分解生成的二氧化碳
(2)①证明分解产物中有CO2的现象是装置B中澄清石灰水变浑浊
②证明分解产物中有CO的现象是装置D中澄清石灰水不变浑浊,装置F中黑色氧化铜变为红色固体,装置G中澄清石灰水变浑浊
(3)实验结束后,装置F中黑色氧化铜变为红色固体.简述检验红色固体中是否含有Cu2O的实验方法(已知Cu2O溶于稀硫酸生成铜单质和硫酸铜):取少量固体与试管中,加稀硫酸,若溶液变蓝色,说明有Cu2O,若溶液不变色,则不含有Cu2O
(4)①草酸和草酸钠(Na2C2O4)可以在酸性条件下被KMnO4、MnO2氧化.KMnO4和草酸钠在稀硫酸中反应的离子方程式是2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O.
②实验室常用草酸钠标定KMnO4溶液.操作如下:准确称取0.2000g草酸钠,放入锥形瓶中,加100mL稀硫酸溶解,用配置好的KMnO4溶液滴定.当加入1滴KMnO4溶液后,锥形瓶中溶液立即由无色变为紫红色,且30s不褪色,即达到滴定终点.重复上述滴定操作三次,实验数据如下表所示.
| 滴定前 | 第一次终点 | 第二次终点 | 第三次终点 | |
| 滴定管 液面刻度 | 0.00mL | 16.02mL | 16.00mL | 16.01mL |
9.下列变化规律正确的是( )
| A. | 半径:Li>Na>K>Rb | |
| B. | 酸性:HClO4>H2SO4>H3PO4>H2CO3 | |
| C. | 气态氢化物的稳定性:HI>HBr>HCl>HF | |
| D. | 还原性:Cl->Br->I->S2- |
6.HClO是比H2CO3还弱的酸,为了提高氯水中HClO的浓度,可加入( )
| A. | H2O | B. | CaO(s) | C. | CaCO3 (s) | D. | NaOH (s) |
3.在Zn+HNO3→Zn(NO3)2+NH4NO3+H2O的反应中,如果2mol Zn完全起反应,则被还原的HNO3的物质的量是( )
| A. | 0.5mol | B. | 1mol | C. | 2mol | D. | 5mol |
4.根据原子结构及元素周期律的知识,下列叙述正确的是( )
| A. | 标准状况下,HF为液态,是因为氢氟键很稳定 | |
| B. | N最外层有5个电子,所以负化合价只有-3价 | |
| C. | 硅和锗处于金属与非金属的过渡位置,硅和锗都可用作半导体材料 | |
| D. | Cl-、S2-、Ca2+、K+半径逐渐减小 |
 NH4++NH2-.
NH4++NH2-.