题目内容
10.对如图所示装置,叙述正确的是( )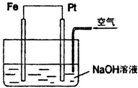
| A. | Fe是正极,Pt是负极 | B. | 该装置中,电子从Fe流向Pt | ||
| C. | 正极反应为:2H++2e-═H2↑ | D. | 负极反应为:4OH--4e-═2H2O+O2↑ |
分析 A、原电池中,一般是不活泼金属为正极,活泼金属为负极;
B、原电池中,电子从负极流向正极;
C、原电池中,一般是不活泼金属为正极;
D、原电池的负极上发生失电子的氧化反应.
解答 解:A、原电池中,一般是不活泼金属为正极,活泼金属为负极,所以Fe是负极,Pt是正极,故A错误;
B、该原电池中,电子从负极铁流向正极Pt,故B正确;
C、Pt为正极,其电极反应为氧气发生得电子的还原反应:2H2O+O2+4e-=4OH-,故C错误;
D、原电池的负极上是金属铁发生失电子的氧化反应,即Fe-2e-=Fe2+,故D错误.
故选:B.
点评 本题考查学生金属铁的吸氧腐蚀知识,注意原电池工作原理的应用知识,难度不大.

练习册系列答案
相关题目
5.下列各组物质中全部是弱电解质的是( )
| A. | NH3、Cl2、H3PO4 | B. | AgCl、Ba(OH)2、H2S | ||
| C. | H2SO3、NaOH、H2SO4 | D. | NH3•H2O、H2O、CH3COOH |
2.下列叙述正确的是( )
| A. | 不能跟酸反应的氧化物一定能跟碱反应 | |
| B. | 同一主族元素的氢化物,相对分子质量越大,它的沸点一定越高 | |
| C. | 在CCl4、PCl3、HCl中各原子最外层均能达到8电子稳定结构 | |
| D. | 升高温度可以加快反应速率,其主要原因是反应物分子能量增加,活化分子百分数的增加,使有效碰撞次数增加 |
19.下列关于铝的叙述,不正确的是( )
| A. | 铝属于ⅢA族元素 | B. | 铝既能溶于酸,又能溶于强碱溶液 | ||
| C. | 在常温下,铝不能与氧气反应 | D. | 铝是地壳中含量最多的金属元素 |
20.有一块镁铝合金,其中镁与铝的质量比是8:9.加入足量稀HNO3使其完全溶解后,产生NO气体在标准状况下的体积为11.2L,溶液中再加入NaOH溶液,生成沉淀质量的最大值为( )
| A. | 17.4g | B. | 46.8g | C. | 40.8g | D. | 23.4g |
 .
.