题目内容
【题目】目前世界上60%的镁是从海水中提取的。已知海水提取镁的主要步骤如图:
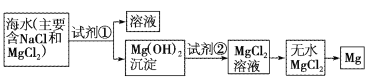
(1)关于加入试剂①作沉淀剂,有以下几种不同方法,请完成下列问题。
方法 | 是否正确 | 简述理由 |
方法1:直接往海水中加入沉淀剂 | 不正确 | 海水中镁离子浓度小,沉淀剂的用量大,不经济 |
方法2:高温加热蒸发海水后,再加入沉淀剂 | 不正确 | (一) |
你认为最合理的其他方法是:(二) | ||
(一)___;
(二)___;
(2)框图中加入的试剂①应该是___(填化学式);加入的试剂②是___(填化学式);工业上由无水MgCl2制取镁的化学方程式为___。
(3)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是___。
【答案】能源消耗大,不经济 海滩晒盐蒸发浓缩得到苦卤水后,加入沉淀剂 Ca(OH)2 HCl MgCl2(熔融)![]() Mg+Cl2↑ 过滤
Mg+Cl2↑ 过滤
【解析】
本题考查的是从海水中提取镁的流程,试剂①应该是石灰乳,发生的反应为MgCl2+Ca(OH)2===Mg(OH)2↓+CaCl2,经过过滤得到Mg(OH)2沉淀,加入试剂②盐酸,发生反应Mg(OH)2+2HCl===MgCl2+2H2O,然后蒸发浓缩,冷却结晶脱水制的无水MgCl2,再电解熔融的MgCl2便可制得Mg,据此分析解答问题。
(1)高温蒸发海水时消耗能源大,不经济,方法不正确,应先浓缩海水再加入沉淀剂,故答案为:能源消耗大,不经济;海滩晒盐蒸发浓缩得到苦卤水后,加入沉淀剂;
(2)根据上述分析可知,试剂①应该是石灰乳,发生的反应为MgCl2+Ca(OH)2===Mg(OH)2↓+CaCl2,经过过滤得到Mg(OH)2沉淀,加入试剂②盐酸,发生反应Mg(OH)2+2HCl===MgCl2+2H2O,工业上电解熔融的MgCl2便可制得Mg,化学方程式为MgCl2(熔融)![]() Mg+Cl2↑,故答案为:Ca(OH)2;HCl;MgCl2(熔融)
Mg+Cl2↑,故答案为:Ca(OH)2;HCl;MgCl2(熔融)![]() Mg+Cl2↑;
Mg+Cl2↑;
(3)试剂①应该是石灰乳,发生的反应为MgCl2+Ca(OH)2===Mg(OH)2↓+CaCl2,经过过滤得到Mg(OH)2沉淀,故答案为:过滤。

 高中必刷题系列答案
高中必刷题系列答案【题目】重铬酸钠(Na2Cr2O7·2H2O)俗称红矾钠,在工业方面有广泛用途。我国目前主要是以铬铁矿(主要成份为FeO、Cr2O3,还含有Al2O3、MgO、SiO2等杂质)为主要原料进行生产,其主要工艺流程如下:
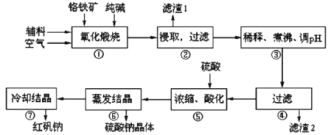
①中涉及的主要反应有:
主反应:4FeO·Cr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
副反应:SiO2+Na2CO3![]() Na2SiO3+CO2↑、Al2O3+Na2CO3
Na2SiO3+CO2↑、Al2O3+Na2CO3![]() 2NaAlO2+CO2↑
2NaAlO2+CO2↑
部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 |
完全沉淀时溶液pH | 4.7 | 3.7 | 11.2 | 5.6 |
试回答下列问题:
(1)“①”中反应是在回转窑中进行,反应时需不断搅拌,其作用是________。
(2)“③”中调节pH至4.7,目的是________。
(3)“⑤”中加硫酸酸化的目的是使![]() 转化为
转化为![]() ,请写出该平衡转化的离子方程式:________。
,请写出该平衡转化的离子方程式:________。
(4)称取重铬酸钠试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶(锥形瓶)中,加入10mL2mol·L-1H2SO4和足量碘化钠(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol·L-1Na2S2O3标准溶液滴定(I2+2![]() =2I-+
=2I-+![]() )。
)。
①判断达到滴定终点的依据是:________;
②若实验中共用去Na2S2O3标准溶液40.00mL,所得产品的中Na2Cr2O7的纯度(设整个过程中其它杂质不参与反应)________。
【题目】酸性![]() 溶液与
溶液与![]() 溶液反应的离子方程式为:
溶液反应的离子方程式为:![]() ,某同学设计如下表所示方案探究温度、浓度改变对该反应速率的影响情况。
,某同学设计如下表所示方案探究温度、浓度改变对该反应速率的影响情况。
实验序号 | 实验温度 | 参加反应的物质 | 溶液颜色褪至无色所需时间 | ||||
|
|
| |||||
|
|
|
|
| |||
A | 298 | 2 |
| 4 | a | 0 |
|
B |
| 2 |
| 3 | a |
| 10 |
C | 318 | 2 |
|
| a | 1 |
|
(1)实验中a的最小值为____________,探究温度变化对反应速率影响情况的两组实验是________。
(2)![]() ____________,
____________,![]() ____________,利用实验B中数据计算,用
____________,利用实验B中数据计算,用![]() 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为![]() ________。
________。
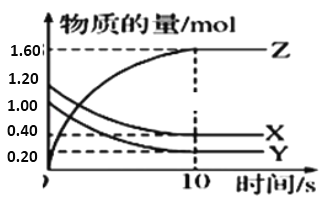
(3)他们发现,A组实验中收集的![]() 体积如图a所示;若使A组反应在绝热容器中进行,该反应的反应速率随着时间的变化如图b所示。
体积如图a所示;若使A组反应在绝热容器中进行,该反应的反应速率随着时间的变化如图b所示。
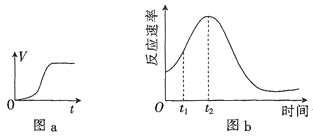
![]() 时间内速率变快的主要原因可能是:一是产物中
时间内速率变快的主要原因可能是:一是产物中![]() 是反应的催化剂;二是______________________________。
是反应的催化剂;二是______________________________。
![]() 由图b信息知,催化剂的催化效果与其用量________
由图b信息知,催化剂的催化效果与其用量________![]() 填“有关”“无关”或“无法确定”
填“有关”“无关”或“无法确定”![]() 。
。