题目内容
14.某一有机物A可发生如图变化:已知C为羧酸,且C、E不发生银镜反应,则A的可能结构有( )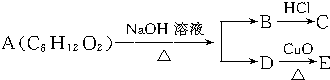
| A. | 4种 | B. | 3种 | C. | 2种 | D. | 1种 |
分析 A能发生水解反应,说明A为酯,A水解生成B、D,D能发生氧化反应,则D是醇、B是羧酸钠、C是羧酸,C、E不发生银镜反应,说明C不是甲酸、E不是醛,结合碳原子守恒判断A的结构,据此分析解答.
解答 解:A能发生水解反应,说明A为酯,A水解生成B、D,D能发生氧化反应,则D是醇、B是羧酸钠、C是羧酸,C、E不发生银镜反应,说明C不是甲酸、E不是醛,
如果C是乙酸,则D可能是2-羟基丁醇、2-甲基-2-羟基丙醇;
如果C是丙酸,则C是2-丙醇,
所以A结构简式可能是CH3COOCH(CH3)CH2CH3、CH3COOC(CH3)3、CH3CH2COOCH(CH3)2,所以有3种结构,故选B.
点评 本题考查有机物推断,侧重考查酯、醇、醛、羧酸之间的转化,知道“C、E不发生银镜反应”的含义是解本题关键,同时考查学生发散思维能力,题目难度不大.

练习册系列答案
相关题目
4.甲、乙两个研究性学习小组为测定氨分子中氮、氢原子个数比,设计如下实验流程:

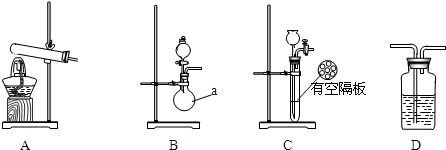
实验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,立即加热氧化铜.反应完毕后,黑色的氧化铜转化为红色的铜.下图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶.
甲小组测得,反应前氧化铜的质量m1g、氧化铜反应后剩余固体的质量m2g、生成氮气在标准状况下的体积V1L.乙小组测得,洗气前装置D的质量m3g、洗气后装置D的质量m4g、生成氮气在标准状况下的体积V2L.
请回答下列问题:
(1)检查A装置气密性的操作是连接导管,将导管插入水中;加热试管,导管口有气泡产生;停止加热,导管内有水回流并形成一段稳定的水柱.
(2)甲、乙两小组选择了不同的方法制取氨气,请将实验装置的字母编号和制备原理填写在下表的空格中.
(3)甲小组用所测得数据计算出氨分子中氮、氢的原子个数之比为5V1:7(m1-m2).
(4)乙小组用所测得数据计算出氨分子中氮、氢的原子个数比明显小于理论值.为此,乙小组在原有实验的基础上增加了一个装有某药品的实验仪器,重新实验.根据实验前后该药品的质量变化及生成氮气的体积,得出了合理的实验结果.该药品的名称是碱石灰(氢氧化钠、氧化钙等).

实验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,立即加热氧化铜.反应完毕后,黑色的氧化铜转化为红色的铜.下图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶.

甲小组测得,反应前氧化铜的质量m1g、氧化铜反应后剩余固体的质量m2g、生成氮气在标准状况下的体积V1L.乙小组测得,洗气前装置D的质量m3g、洗气后装置D的质量m4g、生成氮气在标准状况下的体积V2L.
请回答下列问题:
(1)检查A装置气密性的操作是连接导管,将导管插入水中;加热试管,导管口有气泡产生;停止加热,导管内有水回流并形成一段稳定的水柱.
(2)甲、乙两小组选择了不同的方法制取氨气,请将实验装置的字母编号和制备原理填写在下表的空格中.
| 实验装置 | 实验药品 | 制备原理 | |
| 甲小组 | A | 氢氧化钙、硫酸铵 | 反应的化学方程式为① (NH4)2SO4+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaSO4. |
| 乙小组 | ②B | 浓氨水、氢氧化钠 | 用化学平衡原理分析氢氧化钠的作用: ③氢氧化钠溶于氨水后放热,增加氢氧根浓度,使NH3+H2O?NH3•H2O?NH4++OH-向逆反应方向移动,加快氨气逸出. |
(4)乙小组用所测得数据计算出氨分子中氮、氢的原子个数比明显小于理论值.为此,乙小组在原有实验的基础上增加了一个装有某药品的实验仪器,重新实验.根据实验前后该药品的质量变化及生成氮气的体积,得出了合理的实验结果.该药品的名称是碱石灰(氢氧化钠、氧化钙等).
5.下列叙述正确的是( )
| A. | 无论是纯水还是酸性、碱性或中性稀溶液,常温下,其c(H+)•c(OH-)=1×10-14 | |
| B. | 某溶液由水电离出的c(OH-)=10-a mol/L,若a>7时,则该溶液的pH一定为14-a | |
| C. | 0.2 mol/L CH3COOH溶液中的c(H+)是0.1 mol•L-1 CH3COOH溶液中的c(H+)的2倍 | |
| D. | 任何浓度的溶液都可以用pH来表示其酸性的强弱 |