题目内容
2.(1)在25℃、101kPa下,1g甲烷燃烧生成CO2和液态水时放热55.6kJ.则表示甲烷燃烧热的热化学方程式CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-889.6kJ/mol.(2)盖斯定律在生产和科学研究中有很重要的意义.有些反应的反应热虽然无法直接测得,但可通过间接的方法测定.金红石(TiO2)制钛,涉及的步骤为:
TiO2-TiCl4-Ti,已知:C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol ①
O2(g)+2CO(g)=2CO2 (g)△H=-566kJ/mol ②
TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g)△H=+141kJ/mol ③
写出金红石与氯气、石墨制取TiCl4(s)和CO的热化学反应方程式TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)△H=-80KJ/mol.
分析 (1)燃烧热是指在25℃、101kPa下,1mol纯净物完全燃烧生成稳定的氧化物放出的热量,表示燃烧热的热化学方程式中可燃物的物质的量必须为1mol,产物必须为稳定氧化物;
(2)根据盖斯定律进行计算,由③+①×2-②得出正确结论.
解答 解:(1)在25℃、101kPa下,1g甲烷燃烧生成CO2和液态水时放热55.6kJ,则16g甲烷完全燃烧生成二氧化碳和液态水放出的热量为16×55.6KJ=889.6KJ,
则甲烷燃烧热的热化学方程式为CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-889.6KJ•mol-1,
故答案为:CH4(g)+2O2 (g)=CO2 (g)+2H2O(l)△H=-889.6kJ/mol;
(2)C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol ①
O2(g)+2CO(g)=2CO2 (g)△H=-566kJ/mol ②
TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g)△H=+141kJ/mol ③
由③+①×2-②得TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)△H=141kJ/mol+(-393.5kJ/mol)×2-(-566kJ/mol)=-80KJ/mol,
故答案为:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)△H=-80KJ/mol.
点评 本题考查燃烧热的热化学方程式的书写及盖斯定律的应用,难度不大.注意表示燃烧热的热化学方程式,可燃物为1mol,生成物为稳定的氧化物.

练习册系列答案
 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
12.某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率.请回答下列问题:
(1)硫酸铜溶液可以加快氢气生成速率的原因是CuSO4与Zn反应产生的Cu与Zn形成Cu-Zn原电池,加快了氢气生成的速率
(2)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是Ag2SO4;
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间.
①请完成此实验设计,其中:V1=30,V6=10,V9=17.5;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因是当加入的CuSO4溶液超过一定量时,生成的单质Cu会沉积在Zn的表面,降低了Zn与溶液的接触面积.
(1)硫酸铜溶液可以加快氢气生成速率的原因是CuSO4与Zn反应产生的Cu与Zn形成Cu-Zn原电池,加快了氢气生成的速率
(2)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是Ag2SO4;
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间.
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol/L H2SO 4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因是当加入的CuSO4溶液超过一定量时,生成的单质Cu会沉积在Zn的表面,降低了Zn与溶液的接触面积.
13.下列说法中,正确的是( )
| A. | 除去液溴中少量的氯水,可向其中加少量KI | |
| B. | 氯水和氯气均能使湿润的有色布条褪色,都是HClO作用的结果 | |
| C. | 某白色晶体与NaOH浓溶液混合,有能使湿润红色石蕊试纸变蓝的气体产生,则该晶体一定是NH4Cl | |
| D. | 某溶液能使淀粉碘化钾试纸变蓝,则溶液中一定含有Cl2 |
10.甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系:甲$\stackrel{丁}{→}$乙$?_{甲}^{丁}$丙.下列有关物质的推断不正确的是( )
| A. | 若甲为焦炭,则丁可能是O2 | B. | 若甲为SO2,则丁可能是NaOH溶液 | ||
| C. | 若甲为Fe,则丁可能是盐酸 | D. | 若甲为NaOH溶液,则丁可能是CO2 |
17.11.2L甲烷、乙烷、甲醛组成的混合气体,完全燃烧后生成15.68LCO2(气体体积均在标准状况下测定),混合气体中乙烷的体积百分含量为( )
| A. | 20% | B. | 40% | C. | 60% | D. | 80% |
7.如图为元素周期表截取的短周期的一部分,即 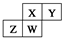 .四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
.四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
 .四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
.四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )| A. | 原子半径:W>Z>Y>X | |
| B. | 气态氢化物的稳定性:Z>W>X>Y | |
| C. | W的最高正化合价与最低负化合价的绝对值可能相等 | |
| D. | Z的最高价氧化物的水化物可能为强碱 |
14.某一有机物A可发生如图变化:已知C为羧酸,且C、E不发生银镜反应,则A的可能结构有( )
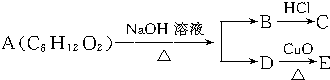
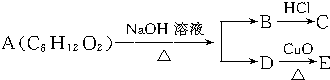
| A. | 4种 | B. | 3种 | C. | 2种 | D. | 1种 |
 ,1个O22+中含有2个π键.
,1个O22+中含有2个π键.