题目内容
【题目】Ⅰ. 由中科院等离子体物理研究所自主研制的全超导托卡马克实验装置(俗称“人造太阳”)正在接受技术升级。人造太阳是利用氘、氚核聚变反应释放巨大能量原理而实现的。下列说法正确的是________。
A.氕、氘、氚三种元素在周期表中的位置不同
B.20 g D2O含有的中子数为6.02×1024个
C.在隔绝空气和高温下LiCl与金属钠反应可获得金属锂
Ⅱ. 部分元素在周期表中的位置如下:
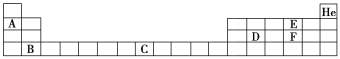
请回答下列问题:
(1)元素C在周期表中的位置为________。
(2)判断E和F对应的简单氢化物沸点高低,并解释原因____________。
(3)用电子式表示F的氢化物的形成过程:___________。
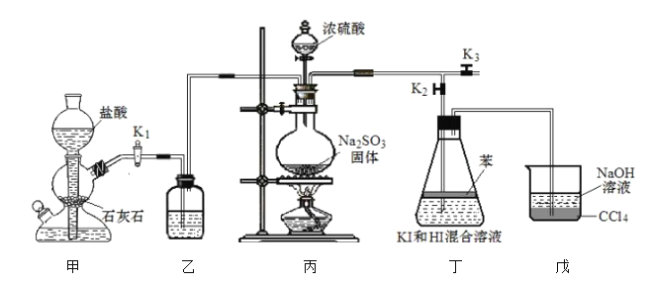
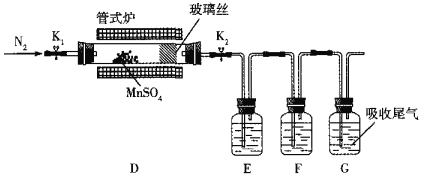
Ⅲ.溴及其化合物广泛用于医药、塑料阻燃剂等,苦卤提溴的工业流程如下:

(1)结合元素周期律解释Cl的非金属性强于Br的原因:_______________。
(2)吸收塔中,A吸收了Br2后的溶液中含有Br和BrO3,则A是________(填序号)。
A.NaCl溶液 B.Na2CO3溶液 C.SO2气体
(3)从吸收塔出来的溶液中加入稀H2SO4得到Br2的离子方程式是______。
【答案】BC 第四周期Ⅷ族 H2O沸点高,水分子可形成分子间氢键作用力强,故沸点高 ![]() Cl和Br均为第ⅦA族元素,原子最外层电子数均为7,电子层数Cl<Br,原子半径Cl<Br,得电子能力Cl>Br,非金属性Cl>Br B 5Br+ BrO3 + 6H+ =3Br2 + 3H2O
Cl和Br均为第ⅦA族元素,原子最外层电子数均为7,电子层数Cl<Br,原子半径Cl<Br,得电子能力Cl>Br,非金属性Cl>Br B 5Br+ BrO3 + 6H+ =3Br2 + 3H2O
【解析】
A.氕、氘、氚三种元素为H的同位素,质子数相同;
B.D2O的摩尔质量为20g/mol,则20g D2O即1mol;
C.还原性:Na>Li,在隔绝空气和高温下LiCl与金属钠反应可获得金属锂;
Ⅱ.根据元素周期表的信息,A为Li,B为Ca,C为Fe,D为Si,E为O,F为S。
Ⅲ.苦卤中的溴离子与氯气反应生成溴,在吹出塔经热空气吹出溴蒸气,在吸收塔吸收,生成Br和BrO3,再与稀硫酸反应生成单质溴。
A.氕、氘、氚三种元素为H的同位素,质子数相同,则在周期表中的位置相同,A错误;
B.D2O的摩尔质量为20g/mol,则20g D2O即1mol,1mol D2O含有的中子的物质的量为10mol,所以1mol含有的中子数为6.02×1024个,B正确;
C.还原性:Na>Li,在隔绝空气和高温下LiCl与金属钠反应可获得金属锂,C正确;
答案为BC;
II.(1)元素C为Fe,位于第四周期Ⅷ族;
(2)E和F分别为O、S,氢化物为H2O、H2S,水分子间可形成氢键,导致分子间的作用力增大,熔沸点升高,则H2O沸点高;
(3)F的氢化物为H2S,电子式表示其形成过程为![]() ;
;
III.(1)Cl、Br属于同一主族,最外层均有7个电子,Cl原子核外有3个电子层,Br有4个电子层,则原子半径Cl<Br,原子核对核外电子的作用力Cl>Br,得电子能力Cl>Br,则非金属性:Cl>Br;
(2)Br2在碱性溶液中生成Br和BrO3,结合题中给定试剂,答案为B;
(3)Br和BrO3,在酸性条件下生成溴和水,反应的离子方程式为5Br+BrO3+6H+ =3Br2+ 3H2O。

【题目】某同学用KSCN溶液和FeCl2溶液探究Fe2+的还原性时出现异常现象,实验如下:
① | ② | ③ |
|
|
|
溶液变红,约10秒后红色褪去,产生能使带火星木条复燃的气体,取褪色后溶液,滴加盐酸和BaCl2溶液,产生白色沉淀 | 溶液变红且不褪色,有能使带火星木条复燃的气体产生,产物经检验有丁达尔效应 | 溶液变红且不褪色,滴加盐酸和BaCl2溶液,无白色沉淀,产物经检验无丁达尔效应 |
下列说法错误的是
A.②中红色溶液中含有Fe(OH)3胶体
B.实验②中发生的氧化还原反应只有两种
C.对比①②,可以判定酸性条件下H2O2可以氧化SCN-
D.③中发生的氧化还原反应为:4Fe2++O2+4H+=4Fe3++2H2O
【题目】铅酸蓄电池价格低廉,原材料易得,适用范围广。其放电时的反应原理为:
Pb+PbO2+2H2SO4===2PbSO4+2H2O。

(1) 写出铅酸蓄电池放电时正极的电极反应式:________,放电时,H+向电池______极定向移动(填“正”或“负”)。
(2) 传统的铅酸蓄电池在充电末期,电极上会产生O2,为了避免气体逸出形成酸雾腐蚀设备,科学家发明了密封铅蓄电池(VRLA),采用阴极吸收法达到密封效果。其原理如图所示,则O2在阴极被吸收的电极反应式为________。
(3) 铅的电解精炼是工业上实现废铅回收以及粗铅提纯的重要手段。铅的电解精炼在由PbSiF6和H2SiF6两种强电解质组成的水溶液中进行。从还原炉中产出的某粗铅成分如下表所示:
成分 | Pb | Cu | Ag | Fe | Zn | Sn | 其它 |
% | 97.50 | 1.22 | 0.12 | 0.15 | 0.09 | 0.64 | 0.28 |
①电解精炼时阳极泥的主要成分是________(元素符号)。
②电解后阴极得到的铅中仍含有微量的杂质,该杂质最有可能是________(填一种)。
③电解过程中,粗铅表面会生成SiF6气体,写出该电极反应式________。