题目内容
【题目】铅酸蓄电池价格低廉,原材料易得,适用范围广。其放电时的反应原理为:
Pb+PbO2+2H2SO4===2PbSO4+2H2O。

(1) 写出铅酸蓄电池放电时正极的电极反应式:________,放电时,H+向电池______极定向移动(填“正”或“负”)。
(2) 传统的铅酸蓄电池在充电末期,电极上会产生O2,为了避免气体逸出形成酸雾腐蚀设备,科学家发明了密封铅蓄电池(VRLA),采用阴极吸收法达到密封效果。其原理如图所示,则O2在阴极被吸收的电极反应式为________。
(3) 铅的电解精炼是工业上实现废铅回收以及粗铅提纯的重要手段。铅的电解精炼在由PbSiF6和H2SiF6两种强电解质组成的水溶液中进行。从还原炉中产出的某粗铅成分如下表所示:
成分 | Pb | Cu | Ag | Fe | Zn | Sn | 其它 |
% | 97.50 | 1.22 | 0.12 | 0.15 | 0.09 | 0.64 | 0.28 |
①电解精炼时阳极泥的主要成分是________(元素符号)。
②电解后阴极得到的铅中仍含有微量的杂质,该杂质最有可能是________(填一种)。
③电解过程中,粗铅表面会生成SiF6气体,写出该电极反应式________。
【答案】PbO2+2e-+SO42-+4H+ ===PbSO4+2H2O 正 O2+4H++4e- ===2H2O Cu、Ag Sn SiF62--2e- === SiF6
【解析】
(1)根据铅酸蓄电池电池的反应原理Pb+PbO2+2H2SO4===2PbSO4+2H2O,放电时,正极的PbO2得到电子,分析写出正极电极反应式,H+带正电荷向电池正极移动;
(2)由题中所给的图可知,O2在阴极失去电子和溶液中的H+生成水;
(3)①电解精炼时阳极泥的主要成分是金属活动性比铅弱的铜和银;
②电解后阴极得到的铅中仍含有微量的杂质,该杂质最有可能是与铅活动性最接近的锡;
③电解过程中,粗铅作阳极,在粗铅表面生成SiF6气体的电极反应式为:SiF62--2e-= SiF6。
(1)根据铅酸蓄电池电池的反应原理Pb+PbO2+2H2SO4===2PbSO4+2H2O,放电时,正极的PbO2得到电子,发生还原反应,正极电极反应式为:PbO2+2e-+SO42-+4H+ ===PbSO4+2H2O,H+带正电荷向电池正极移动;
本题答案为:PbO2+2e-+SO42-+4H+ ===PbSO4+2H2O,正。
(2)由图可知,O2在阴极失去电子和溶液中的H+生成水,则O2在阴极被吸收的电极反应式为:O2+4H++4e- =2H2O;
本题答案为:O2+4H++4e- =2H2O。
(3)①电解精炼时阳极泥的主要成分是金属活动性比铅弱的铜和银;
本题答案为:Cu、Ag。
②电解后阴极得到的铅中仍含有微量的杂质,该杂质最有可能是与铅活动性最接近的锡;
本题答案为:Sn。
③电解过程中,粗铅作阳极,在粗铅表面生成SiF6气体的电极反应式为:SiF62--2e-= SiF6;
本题答案为:SiF62--2e- = SiF6。

 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案【题目】温度为T 时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,
反应:PCl5(g)![]() PCl3(g)+Cl2(g)经一段时间后达到平衡,反应过程中测定的部分数据见下表:
PCl3(g)+Cl2(g)经一段时间后达到平衡,反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 250 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
下列说法正确的是
A. 反应在前50 s内的平均速率v(PCl3)=0.0032mol/(L·s)
B. 保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol/L,该反应为放热反应
C. 相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,达到平衡前的v正>v逆
D. 相同温度下,起始时向容器中充入2.0 mol PCl3、2.0 mol Cl2,达到平衡时,PCl3的转化率小于80%
【题目】实验室以苯甲醛为原料制备间溴苯甲醛的反应如下:
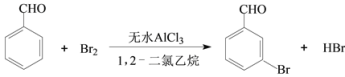
已知:(1)间溴苯甲醛温度过高时易被氧化。
(2)溴、苯甲醛、1,2-二氯乙烷、间溴苯甲醛的沸点见下表:
物质 | 溴 | 苯甲醛 | 1,2-二氯乙烷 | 间溴苯甲醛 |
沸点/℃ | 58.8 | 179 | 83.5 | 229 |
步骤1:将一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后装入三颈烧瓶(如右图所示),缓慢滴加经浓硫酸干燥过的足量液溴,控温反应一段时间,冷却。

步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机层用10% NaHCO3溶液洗涤。
步骤3:经洗涤的有机层加入适量无水MgSO4固体,放置一段时间后过滤出
MgSO4nH2O晶体。
步骤4:减压蒸馏有机层,收集相应馏分。
(1)实验装置中冷凝管的主要作用是_____,锥形瓶中应为_____(填化学式)溶液。
(2)步骤1反应过程中,为提高原料利用率,适宜的温度范围为(填序号)_______。
A.>229℃ B.58.8℃~179℃ C.<58.8℃
(3)步骤2中用10% NaHCO3溶液洗涤,是为了除去溶于有机层的___(填化学式)。
(4)步骤3中加入无水MgSO4固体的作用是_____。
(5)步骤4中采用减压蒸馏,是为了防止______。
(6)若实验中加入了5.3 g苯甲醛,得到3.7 g间溴苯甲醛。则间溴苯甲醛产率为______。

