题目内容
10.下列两个反应的类型相同的是( )| A. | 由乙炔制氯乙烯;甲烷与氯气在光照条件下反应 | |
| B. | 溴乙烷和氢氧化钠乙醇溶液共热;乙醇制得乙烯 | |
| C. | 乙烯使溴的四氯化碳溶液褪色;乙烯使酸性高锰酸钾溶液褪色 | |
| D. | 溴乙烷和氢氧化钠溶液共热;乙烯和氢气反应 |
分析 A.乙炔和氯化氢加成生成氯乙烯,甲烷与氯气光照下发生取代反应;
B.溴乙烷和氢氧化钠乙醇溶液共热为消去反应,乙醇制得乙烯为消去反应;
C.能使溴水褪色,为加成反应,而使酸性高锰酸钾溶液褪色为氧化反应;
D.溴乙烷和氢氧化钠溶液共热为取代反应,乙烯和氢气反应为加成反应.
解答 解:A.乙炔和氯化氢加成生成氯乙烯,甲烷与氯气光照下发生取代反应,反应类型不同,故A不选;
B.溴乙烷和氢氧化钠乙醇溶液共热为消去反应,乙醇制得乙烯为消去反应,反应类型相同,故选B;
C.能使溴水褪色,为加成反应,而使酸性高锰酸钾溶液褪色为氧化反应,反应类型不同,故C不选;
D.溴乙烷和氢氧化钠溶液共热为取代反应,乙烯和氢气反应为加成反应,反应类型不同,故D不选.
故选B.
点评 本题考查有机物的结构与性质,侧重有机反应类型的考查,熟悉烯烃、烷烃的性质及常见有机反应类型即可解答,题目难度不大

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
3.下列说法正确的是( )
| A. | 液面在“0”刻度时,50 mL碱式滴定管和25 mL碱式滴定管所盛液体的体积,其比值一定为2:1 | |
| B. | 将NaOH溶液和氨水溶液各稀释一倍,两者的OH-浓度均减少到原来的二分之一 | |
| C. | 如果盐酸的浓度是醋酸浓度的二倍,则盐酸的H+浓度也是醋酸的二倍 | |
| D. | 制取TiO2可用TiCl4加大量水,同时加热:TiCl4+(x+2)H2O(过量)?TiO2•xH2O↓+4HCl,所得的TiO2•H2O经焙烧得TiO2 |
4.反应①和②分别是从海藻灰和某种矿石中提取碘的主要反应
①2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2
②2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2.
下列说法正确的是( )
①2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2
②2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2.
下列说法正确的是( )
| A. | 两个反应中均为硫元素被氧化 | |
| B. | 反应①、②中生成等量的I2时转移电子数比为1:5 | |
| C. | 氧化性:MnO2>SO42->IO3->I2 | |
| D. | 碘元素在反应①中被还原,在反应②中被氧化 |
2.下列各种说法正确的是( )
①在水中氢、氧原子间均以化学键相结合
②金属和非金属化合时一定形成离子键
③离子键是阳离子、阴离子的相互吸引力
④冰的密度比水的密度小,这与氢键有关
⑤根据电离方程式HCl═H++Cl-,推断HCl分子里存在离子键.
①在水中氢、氧原子间均以化学键相结合
②金属和非金属化合时一定形成离子键
③离子键是阳离子、阴离子的相互吸引力
④冰的密度比水的密度小,这与氢键有关
⑤根据电离方程式HCl═H++Cl-,推断HCl分子里存在离子键.
| A. | ①⑤ | B. | 都不正确 | C. | ④ | D. | ⑤ |
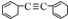 的不饱和度为( )
的不饱和度为( )