题目内容
2.下列各种说法正确的是( )①在水中氢、氧原子间均以化学键相结合
②金属和非金属化合时一定形成离子键
③离子键是阳离子、阴离子的相互吸引力
④冰的密度比水的密度小,这与氢键有关
⑤根据电离方程式HCl═H++Cl-,推断HCl分子里存在离子键.
| A. | ①⑤ | B. | 都不正确 | C. | ④ | D. | ⑤ |
分析 ①在水中氢、氧原子间存在化学键和氢键;
②金属和非金属化合不一定形成离子键,可能形成共价键;
③离子键的实质是阳离子、阴离子间的相互作用力;
④冰中存在氢键,具有方向性和饱和性,其体积变大;
⑤HCl能电离出氢离子和氯离子,但HCl中只存在共价键.
解答 解:①在水中的每个水分子中H原子和O原子之间存在共价键,但水分子之间存在氢键,故错误;
②金属和非金属化合不一定形成离子键,可能形成共价键,如氯化铝,故错误;
③离子键的实质是阳离子、阴离子间的相互作用力,包含吸引力和排斥力,故错误;
④冰中存在氢键,具有方向性和饱和性,其体积变大,则相同质量时冰的密度比液态水的密度小,故正确;
⑤HCl能电离出氢离子和氯离子,但HCl中H原子和Cl之间以共价键相结合,属于共价键,所以只存在共价键,故错误.
故选C.
点评 本题考查化学键,为高频考点,侧重考查基本概念,明确离子键、共价键及离子化合物、共价化合物的关系即可解答,易错选项是⑤.

练习册系列答案
相关题目
15.已知5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O,下列说法不正确的是( )
| A. | KClO3是氧化剂 | |
| B. | 被氧化与被还原的氯元素的质量比为5:1 | |
| C. | Cl2既是氧化产物又是还原产物 | |
| D. | 0.1mol KClO3 参加反应时有1mol电子转移 |
13.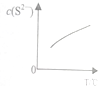 硫粉不溶于水、微溶于酒精,却易溶于Na2S溶液,发生如下反应:(x-1)S(s)+S2-(aq)?Sx2-(aq)(x≤6),达到平衡后,C(S2-)随温度T的变化如图所示.下列有关说法正确的是( )
硫粉不溶于水、微溶于酒精,却易溶于Na2S溶液,发生如下反应:(x-1)S(s)+S2-(aq)?Sx2-(aq)(x≤6),达到平衡后,C(S2-)随温度T的变化如图所示.下列有关说法正确的是( )
 硫粉不溶于水、微溶于酒精,却易溶于Na2S溶液,发生如下反应:(x-1)S(s)+S2-(aq)?Sx2-(aq)(x≤6),达到平衡后,C(S2-)随温度T的变化如图所示.下列有关说法正确的是( )
硫粉不溶于水、微溶于酒精,却易溶于Na2S溶液,发生如下反应:(x-1)S(s)+S2-(aq)?Sx2-(aq)(x≤6),达到平衡后,C(S2-)随温度T的变化如图所示.下列有关说法正确的是( )| A. | 反应(x-1)S(s)+S2-(aq)?Sx2-(aq)的△H>0 | |
| B. | 该反应的平衡常数随温度的升高而减小 | |
| C. | 其他条件不变时,向平衡后的溶液中再加入硫粉,可使溶液中c(Sx2-)增大 | |
| D. | 依此原理,常温下Cl2在饱和NaCl溶液中的溶解度也比在水中的大 |
10.下列两个反应的类型相同的是( )
| A. | 由乙炔制氯乙烯;甲烷与氯气在光照条件下反应 | |
| B. | 溴乙烷和氢氧化钠乙醇溶液共热;乙醇制得乙烯 | |
| C. | 乙烯使溴的四氯化碳溶液褪色;乙烯使酸性高锰酸钾溶液褪色 | |
| D. | 溴乙烷和氢氧化钠溶液共热;乙烯和氢气反应 |
17.某元素的一种核素X的原子质量数为A,含N个中子,它与1H原子组成HmX分子,在a g HmX分子中含质子的物质的量是( ) mol.
| A. | $\frac{a}{A+m}$(A-N+m) | B. | $\frac{a}{A}$(A-N) | C. | $\frac{a}{A+m}$(A-N) | D. | $\frac{a}{A}$(A-N+m) |
7.C5H12有3种不同结构:甲CH3(CH2)3CH3,乙CH3CH(CH3)CH2CH3,丙C(CH3)4.下列相关叙述正确的是( )
| A. | 甲、乙、丙属同系物均可与氯气、溴蒸气发生取代反应 | |
| B. | C5H12表示一种纯净物 | |
| C. | 甲、乙、丙中,丙的沸点最低 | |
| D. | 乙有3种不同沸点的二氯取代物 |
14.下列分子中所有原子都满足最外层8电子稳定结构的是( )
| A. | 六氟化氙(XeF6) | B. | 次氯酸(HClO) | C. | 二氧化碳(CO2) | D. | 三氟化硼(BF3) |
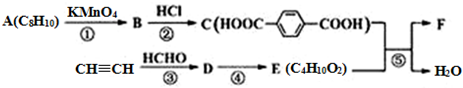
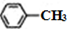 $\stackrel{KMnO_{4}}{→}$
$\stackrel{KMnO_{4}}{→}$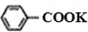
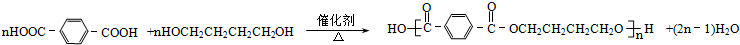 .
.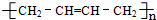
 CO(g)+H2(g)当增加反应物物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g)当增加反应物物质的量时,平衡一定向正反应方向移动