题目内容
4.按要求写出下列方程式(1)铜与浓硫酸反应的化学方程式Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O
(2)NaAlO2溶液与NaHCO3 溶液混合的离子方程式AlO2-+HCO3-+H2O═Al(OH)3↓+CO32-
(3)Na2O2与水反应的离子方程式2Na2O2+2H2O═4Na++OH-+O2↑.
分析 (1)铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫和水;
(2)NaHCO3溶液与NaAlO2溶液混合产生白色沉淀氢氧化铝;
(3)过氧化钠和水反应生成氢氧化钠和氧气.
解答 解:(1)铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫和水,反应的方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(2)NaHCO3溶液与NaAlO2溶液混合产生白色沉淀氢氧化铝和碳酸根离子,反应为:AlO2-+HCO3-+H2O═Al(OH)3↓+CO32-,
故答案为:AlO2-+HCO3-+H2O═Al(OH)3↓+CO32-;
(3)Na2O2与水反应生成NaOH和氧气,离子反应为:2Na2O2+2H2O═4Na++4OH-+O2↑,
故答案为:2Na2O2+2H2O═4Na++4OH-+O2↑.
点评 本题考查了化学方程式、离子方程式的书写,是高考常见题型,题目难度不大,熟悉化学反应的实质是书写离子方程式的关键.

练习册系列答案
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
14.已知某饱和NaCl溶液的体积为vmL,密度为ρg/cm3,质量分数为w%,物质的量的浓度为cmol/L,溶液中含有NaCl的质量为mg,下列说法不正确的是( )
| A. | c=$\frac{2000m}{117v}$mol/L | B. | ρ=$\frac{117c}{20w}$g/mL | ||
| C. | w%=$\frac{117c}{2000ρ}$ | D. | m=1000ρv.w% |
15.NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1mol氢氧根离子与1mol羟基所含电子数均为l0NA | |
| B. | 2.8gN2和CO的混合物中,所含分子总数为0.2NA | |
| C. | 标准状况下,11.2L甲醛气体所含σ键数目为1.5NA | |
| D. | 2.24LC02与足量的Na202反应,转移的电子总数必为0.1NA |
12.能产生“丁达尔效应”的是( )
| A. | 饱和食盐水 | B. | Fe(OH)3胶体 | C. | 盐酸 | D. | 硫酸铜溶液 |
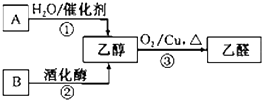 气态烃A中碳元素与氢元素的质量比为6:1.淀粉在一定条件下水解可生成B.B在人体组织中缓慢氧化,放出热量,提供生命活动所需能量.有关物质的转化关系如图:
气态烃A中碳元素与氢元素的质量比为6:1.淀粉在一定条件下水解可生成B.B在人体组织中缓慢氧化,放出热量,提供生命活动所需能量.有关物质的转化关系如图: