题目内容
【题目】一定条件下,向可变容积的密闭容器中通入N2和H2,发生反应:N2(g)+3H2(g)![]() 2NH3(g) △H<0达到平衡后,容器的体积为4L,试回答下列问题:
2NH3(g) △H<0达到平衡后,容器的体积为4L,试回答下列问题:
(1)该条件下,反应的平衡常数表达式K = ,若降低温度,K值将 (填“增大”、“减小”或“不变”)。
(2)达到平衡后,若其它条件不变,把容器体积缩小一半,平衡将___(填“向逆反应方向”、“向正反应方向”或“不”)移动,平衡常数K将 (填“增大”“减小”或“不变”),理由是___________________________。
(3) 达到平衡后,在恒压条件下,向容器中通入氦气(He),氮气的转化率将________(填“增大”、“减小”或“不变”)。
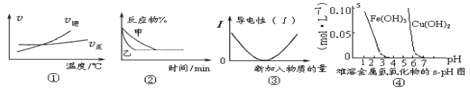
(4)在三个相同的容器中各充入1 molN2和3molH2,在不同条件下分别达到平衡,氨的体积分数ω随时间变化如图。下列说法正确的是 (填序号)。
a.图Ⅰ可能是不同压强对反应的影响,且P2>P1
b.图Ⅱ可能是同温同压下催化剂对反应的影响,且催化性能1>2
c.图Ⅲ可能是不同温度对反应的影响,且T1>T2

(5)常压下,把H2和用He稀释的N2分别通入一个570℃的电解池装置(下图),H2和N2便可在电极上合成氨,装置中的电解质(图中黑细点处)能传导H+,则阴极的电极反应式为___________。

【答案】(1)c2(NH3)/c(N2)·c3(H2),增大;
(2)正,不变,K只与温度有关;
(3)减小;
(4)b;
(5)N2+6e-+6H+=2NH3。
【解析】
试题分析:(1)化学平衡常数:一定条件下,生成物浓度的幂之积和反应物浓度的幂之积,K=c2(NH3)/c(N2)·c3(H2),K只受温度的影响,此反应是放热反应,降低温度,平衡向正反应方向移动,K增大;
(2)缩小容器的体积,增大压强,平衡向正反应方向移动,平衡常数不变,因为平衡常数K只受温度的影响;
(3)恒压下,充入非反应气体,容器体积扩大,各组分的浓度减小,根据勒夏特列原理,平衡应向逆反应方向移动,氮气的转化率减小;
(4)a.根据勒夏特列原理,增大压强,平衡向正反应方向移动,压强越大,NH3的体积分数越大,故错误;b.催化剂只加快反应速率,对化学反应平衡无影响,故正确;c.此反应属于放热反应,根据勒夏特列原理,升高温度,平衡向逆反应方向进行,温度越高,NH3的体积分数越小,故错误;
(5)阴极是得电子,化合价降低,根据装置图,N的化合价降低,N2在阴极上放电,电极反应式为N2+6H++6e-=2NH3。

【题目】现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | 最外层电子数比内层电子总数少4 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 与氢形成的气态化合物在标准状况下的密度为0.76g·L-1 |
Z | 元素最高正价与负价的绝对值之差是6 |
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是 ,在周期表中的位置是 。
(2)元素Y与氢元素形成一种离子YH4+,写出该离子与Z离子形成化合物的电子式 。
(3)写出元素X、T形成的化合物XT2的电子式 。
(4)元素Z与元素T相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 (填序号)。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
d.与铁加热,Z生成三价铁,T生成二价铁
e.T原子与Z原子电子层数相同,Z原子半径小于T原子
(5)T的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为 。
(6)分别用电子式表示Z与镁元素、Y与氮元素形成化合物的过程: 。