题目内容
【题目】合成涤纶的流程图如下所示。
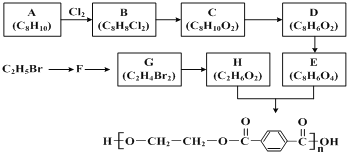
回答下列问题:
(1)B 中官能团的名称是___________________;G的名称是________________;
(2)C→D 的反应类型是________________;
(3)E与 H 反应的化学方程式为________________;
(4)下列说法正确的是_______________;
A.化合物D能发生银镜反应
B.化合物A~D均属于芳香烃
C.反应G→H属于消去反应
D.化合物D能与3molH2发生加成反应
E.化合物C、H、E均能与金属钠反应放出氢气
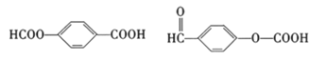
(5)E有多种同分异构体,符合下列条件的同分异构体有_______种,其中在核磁共振氢谱中出现四组峰的是__________________________________(写出结构简式)。
①芳香族化合物;②红外光谱显示含有羧基;③能发生银镜反应;④能发生水解反应
【答案】(1)氯原子 1,2-二溴乙烷
(2)氧化反应
(3)![]()
(4)AE
(5)
【解析】
试题分析:由涤纶结构及H、E的分子式可知,H为HOCH2CH2OH,E为![]() .溴乙烷发生消去反应生成F为CH2=CH2,乙烯与溴发生加成反应生成G为BrCH2CH2Br,1,2-二溴乙烷发生水解反应生成HOCH2CH2OH.A到E的相邻转化中碳骨架不变,结合A的分子式与E的结构可知,A为
.溴乙烷发生消去反应生成F为CH2=CH2,乙烯与溴发生加成反应生成G为BrCH2CH2Br,1,2-二溴乙烷发生水解反应生成HOCH2CH2OH.A到E的相邻转化中碳骨架不变,结合A的分子式与E的结构可知,A为![]() ,对二甲苯与氯气在光照条件下发生侧链上取代反应生成B为
,对二甲苯与氯气在光照条件下发生侧链上取代反应生成B为![]() ,B在氢氧化钠水溶液、加热条件下发生水解反应生成C为
,B在氢氧化钠水溶液、加热条件下发生水解反应生成C为![]() ,C在Cu或Ag作催化剂条件下,发生催化氧化生成D为
,C在Cu或Ag作催化剂条件下,发生催化氧化生成D为![]() ,D发生氧化反应生成
,D发生氧化反应生成![]() ,对苯二甲酸与乙二醇发生缩聚反应得到涤纶为
,对苯二甲酸与乙二醇发生缩聚反应得到涤纶为![]() ;
;
(1)B为![]() ,含有官能团为氯原子;G为BrCH2CH2Br,名称为1,2-二溴乙烷;
,含有官能团为氯原子;G为BrCH2CH2Br,名称为1,2-二溴乙烷;
(2)C→D发生醇的催化氧化生成醛,属于氧化反应;
(3)E与H反应的化学方程式为:
![]() ;
;
(4)A.化合物D为![]() ,含有醛基能发生银镜反应,故A正确;B.化合物A~D中均含有苯环,除B、C、D除C、H元素外还含有O或Cl,属芳香族化合物,不属于芳香烃,故B错误;C.反应G→H属于卤代烃的水解,是取代反应,故C错误;D.化合物D为
,含有醛基能发生银镜反应,故A正确;B.化合物A~D中均含有苯环,除B、C、D除C、H元素外还含有O或Cl,属芳香族化合物,不属于芳香烃,故B错误;C.反应G→H属于卤代烃的水解,是取代反应,故C错误;D.化合物D为![]() 能与5molH2发生加成反应,故D错误;E.化合物C、H、E均含有能与金属钠反应的羧基或醇羟基,可放出氢气,故E正确;答案为AE;
能与5molH2发生加成反应,故D错误;E.化合物C、H、E均含有能与金属钠反应的羧基或醇羟基,可放出氢气,故E正确;答案为AE;
(5)E(![]() )有多种同分异构体,符合下列条件的同分异构体:①芳香族化合物,说明含有苯环;②红外光谱显示含有羧基;③能发生银镜反应,说明含有-CHO,④能发生水解反应,说明含有酯基,可以为-COOH与-OOCH,有邻、间、对3种,可以为-CHO、-OCOOH,有邻、间、对3种,故共有6种,其中在核磁共振氢谱中出现四组峰的是
)有多种同分异构体,符合下列条件的同分异构体:①芳香族化合物,说明含有苯环;②红外光谱显示含有羧基;③能发生银镜反应,说明含有-CHO,④能发生水解反应,说明含有酯基,可以为-COOH与-OOCH,有邻、间、对3种,可以为-CHO、-OCOOH,有邻、间、对3种,故共有6种,其中在核磁共振氢谱中出现四组峰的是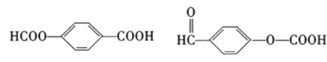 。
。

 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案