��Ŀ����
����Ŀ��ҽ�����̷�(FeSO47H2O)������ȱ����ƶѪ����Чҩ��ij��ѧ��ȤС����̷����������µ�̽����
�������Ʊ���Ʒ��
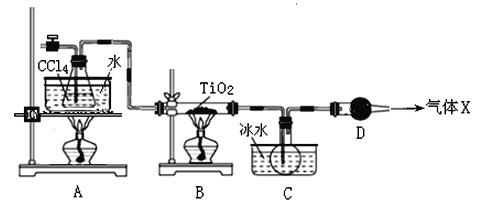
��С���ɷ���м(����������ͭ��������������)������ͼ��ʾװ���Ʊ� FeSO4 7H2O���壬�������£�

��1��Ԥ�������Ƚ�����м���뵽���� Na2CO3��Һ��ϴ�ӣ�Ŀ����__________ ��Ȼ����м��ˮϴ�� 2��3 �顣
��2����ϴ�Ӻ�ķ���м���뵽Բ����ƿ�У�������ͨ��N2
��3���ټ�������ϡ���ᣬ�����¶� 50����80��֮�䣬��ַ�Ӧ��Բ����ƿ��ʣ��Ĺ���Ϊ__________ ��ʵ���ҳ������軯����Һ���鷴Ӧ���ɵ�Fe2+��д���÷�Ӧ�����ӷ�Ӧ����ʽ��______________��
��4����ȡ��Ʒ����������3���з�Ӧ��Ļ�����м�����������ˮ�����ȹ��ˣ���ȴ�ᾧ���˳����壬��������ˮϴ�� 2��3 �Σ�������ֽ���������ɣ��ܱձ��档
�������ⶨFeSO4 7H2O ������
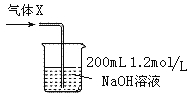
��1����ȡ������Ʒ 10.0g������������ϡ�����У���� 100mL ��Һ��ȷ��ȡ 25.00mL ��Һ������ƿ�У��� 0.1000mol/L KMnO4����Һ�ζ��ζ�3�Σ�ƽ������ 10.00mL��Һ������Ʒ�� FeSO4 7H2O ����������Ϊ________ ��(��֪ Mr(FeSO4 7H2O)=278)��
��2�����������ƫС����������ڶ���ʱ________(����ӡ������ӡ�)������
���𰸡�������1��ϴȥ��м���������
��3��Cu 3Fe2+ +2Fe(CN)63- = Fe3[Fe(CN)6]2 ��
������1��55.6%��2������
��������
���������������1��̼���Ƶ�ˮ��Һ�Լ��ԣ����Գ�ȥ��м��������ۣ�
��3������ͭ�������������ᷴӦ��������ͭ����������������������ͭ����������Ӧ��������������ͭ���ʣ������軯����Һ���鷴Ӧ���ɵ�Fe2+������ɫ�������ɣ�������Ӧ�����ӷ�Ӧ����ʽΪ3Fe2+ +2Fe(CN)63- = Fe3[Fe(CN)6]2 �� ��
���� �ⶨ��Ʒ��Fe2+�ĺ���������������������KMnO4��Һ�ζ���Fe2+��Fe3+����Ԫ�ػ��ϼ�����1�ۣ�MnO4-��Mn2+����Ԫ�ؽ���5�ۣ����ϼ�������С������Ϊ5����Fe2+ϵ��Ϊ5��MnO4- ϵ��Ϊ1������Ԫ���غ��֪Mn2+��Fe3+ϵ���ֱ�Ϊ1��5�����ݵ���غ��֪ȱ��ΪH+��H+��ϵ��Ϊ2+3��5-[2��5-1]=8������HԪ���غ��֪H2Oϵ����4�����Է�Ӧ���ӷ���ʽΪ5Fe2++MnO4-+8H+=1Mn2++5Fe3++4H2O��
��Fe2+�����ʵ���Ϊxmol����
5Fe2+������������MnO4-��
5 1
xmol 0.01L��0.1mol/L
����x=![]() =0.005mol��
=0.005mol��
������Ʒ��FeSO47H2O������0.005mol��4��278g/mol=5.56g������4g��Ʒ��FeSO47H2O����������Ϊ![]() ��100%=55.6%��
��100%=55.6%��
��4������ʱ�������ƫ��Ũ��ƫС��