题目内容
【题目】在Cu + 2H2SO4(浓)![]() CuSO4 + SO2↑+ 2H2O反应中,
CuSO4 + SO2↑+ 2H2O反应中,
(1) 元素被氧化, 是氧化剂,还原产物是 。
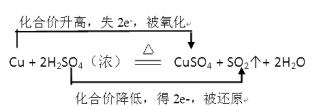
(2)用双线桥标出该反应电子转移的方向和数目。
Cu + 2H2SO4(浓)![]() CuSO4 + SO2↑+ 2H2O
CuSO4 + SO2↑+ 2H2O
(3)若有2mol的H2SO4参与反应,则被还原的H2SO4为 g 。
【答案】(1) 0价的Cu(写Cu的不给分),浓H2SO4 , SO2 (每空1分)
(2)
(3)98g
【解析】
试题分析:(1)反应中单质铜的化合价升高,做还原剂,被氧化,硫酸中的硫化合价降低,做氧化剂,二氧化硫为还原产物。
(2)反应中铜失去2个电子,硫酸中的硫得到2个电子。故线桥表示为:

(3)反应中有2摩尔硫酸参与反应,则有1摩尔硫酸被还原,即98克。

练习册系列答案
 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目