题目内容
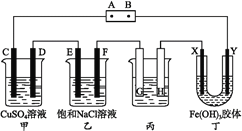
【题目】利用如图所示装置,可以模拟铁的电化学腐蚀,下列说法不正确的是( )

A.若X为碳棒,为减慢铁的腐蚀,开关K应置于N处
B.若X为锌棒,K置于M或N处,均能减慢铁的腐蚀
C.若X为碳棒,将开关K置于M处时铁棒上发生的反应为Fe-2e-=Fe2+
D.若X为锌棒,将开关K置于N处时铁棒上发生的反应为Fe-2e-=Fe2+
【答案】D
【解析】
根据金属的防护,若K置于N处,形成电解池,必须让被保护的金属接电源负极;若开关K置于M处,形成原电池,若要使金属铁被保护,需让铁做正极,据此分析判断。
A.若X为碳棒,当开关K置于N处时,形成电解池,铁做阴极被保护,能减缓铁的腐蚀,故A正确;
B.若X为锌棒,开关K置于M处,形成原电池,锌比铁活泼,锌为负极,铁做正极,在原电池中正极被保护,能减缓铁的腐蚀;当开关K置于N处时,形成电解池,铁做阴极被保护,能减缓铁的腐蚀,故B正确;
C.若X为碳棒,开关K置于M处,形成原电池,铁做负极,铁棒上发生的反应为Fe-2e-=Fe2+,故C正确;
D.当X为锌时,开关K置于N处,形成电解池,铁做阴极,故阴极上的电极反应为:O2+4e-+2H2O=4OH-,故D错误;
故选D。

练习册系列答案
相关题目