��Ŀ����
����Ŀ���� NaClO2�㷺������ֽ��ҵ����ˮ�����ȣ���Ư��������Ư�۵�4~5������ҵ����ClO2������ NaClO2�Ĺ�����������:
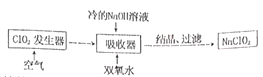
��֪: NaClO2����Һ�ڵ���38��ʱ����NaClO2��3H2O������38��ʱ����NaClO2������˵������ȷ����( )
A.�����еĽᾧ�����˲���Ӧ���������ᾧ�����ȹ���
B.����������еķ�Ӧ�¶ȿ�����߷�Ӧ���ʣ�Ҳ��߷�Ӧ���������
C.�����������ɵ�NaClO2�����ӷ���ʽ:2ClO2+2OH-+H2O2=2ClO2-+O2+2H2O
D.�������з�Ӧ������������ͨ�������Ŀ�������ϳ�ClO2��ʹ�䱻�������
���𰸡�B
��������
A. NaClO2����Һ�ڵ���38��ʱ����NaClO2��3H2O������38��ʱ����NaClO2��������Ӧ�������ᾧ�����ȹ��ˣ�����ȷ��
B.�¶����ߣ�˫��ˮ�ֽ⣬�ʲ�����߷�Ӧ��������ʣ��ʴ���
C.�������ж���������������ƺ������ⷴӦ����NaClO2�����ӷ���ʽ��д��ȷ������ȷ��
D.ͨ������������ϳ��������ȣ�ʹ�䱻������գ�����ȷ��
��ѡB��

 Сѧѧϰ�ð���ϵ�д�
Сѧѧϰ�ð���ϵ�д� Сѧͬ�����������ܾ�ϵ�д�
Сѧͬ�����������ܾ�ϵ�д�����Ŀ������ʵ�����������ͽ��۾���ȷ����
ѡ�� | ʵ����� | ���� | ���� |
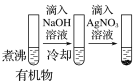
A | ��˫��ˮ�ζ�KI-������Һ | ��Һ���� | �ﵽ�ζ��յ� |
B | ��ʳ�üӵ����м���ʳ��KI��Һ���ټ���CCl4������ | �²���Ϻ�ɫ | ��ʳ�üӵ����к���KIO3 |
C | ��ʪ��ĵ��۵⻯����ֽ����NO2�������� | ��ֽ���� | ������Ϊ������ |
D |
| ����Թ���dz��ɫ���� | �л����к�����ԭ�� |
A. AB. BC. CD. D