题目内容
5.下列推断正确的是( )| A. | SO2、SO3组成元素相同,与H2O反应产物也相同 | |
| B. | 浓硝酸见光会分解,故有时在实验室看到的浓硝酸呈黄色 | |
| C. | CO、NO、NO2都能形成光化学烟雾,是大气污染气体,在空气中都能稳定存在 | |
| D. | 新制氯水显酸性,向新制氯水中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
分析 A.二氧化硫和水反应生成亚硫酸、三氧化硫和水反应生成硫酸;
B.硝酸分解生成二氧化氮、氧气和水,浓硝酸能溶解二氧化氮;
C.氮氧化物是形成光化学烟雾的物质,NO极易被氧气氧化;
D.氯水溶液呈酸性,但次氯酸具有漂白性.
解答 解:A.二氧化硫和水反应生成亚硫酸、三氧化硫和水反应生成硫酸,所以SO2、SO3组成元素相同,与H2O反应产物不同,故A错误;
B.硝酸分解生成二氧化氮、氧气和水,二氧化氮是红棕色气体,浓硝酸溶解了二氧化氮而呈黄色,故B正确;
C.氮氧化物是形成光化学烟雾的物质,NO极易被氧气氧化生成二氧化氮,故C错误;
D.氯水溶液呈酸性,但溶液中的次氯酸具有漂白性,所以向新制氯水中滴加少量紫色石蕊试液,充分振荡后溶液先呈红色后褪色,故D错误;
故选B.
点评 本题考查元素化合物知识,侧重考查物质性质,明确物质发生的反应是解本题关键,易错选项是BD,注意二氧化硫漂白性和次氯酸漂白性原理区别.

练习册系列答案
相关题目
15.下列关于电离度α的叙述中,正确的是( )
①α与浓度无关 ②α值随温度升高而增大 ③在相同条件下,α值的大小可以表示弱电解质的相对强弱 ④α值越大,相应离子浓度一定就越大 ⑤α值增大,相应离子的物质的量一定增大 ⑥在相同条件下,浓度相同的酸,α越大,其酸性也越强.
①α与浓度无关 ②α值随温度升高而增大 ③在相同条件下,α值的大小可以表示弱电解质的相对强弱 ④α值越大,相应离子浓度一定就越大 ⑤α值增大,相应离子的物质的量一定增大 ⑥在相同条件下,浓度相同的酸,α越大,其酸性也越强.
| A. | ①②③ | B. | ①④⑥ | C. | ②③⑥ | D. | ③④⑤ |
16.某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图1).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.
(1)请完成以下实验设计表(表中不要留空格):
(2)编号①实验测得容器中压强随时间变化如图2甲.t2时,容器中压强明显小于起始压强,其原因是铁发生了吸氧腐蚀,请在图2乙中用箭头标出发生该腐蚀时电子流动方向;此时,碳粉表面发生了还原(填“氧化”或“还原”)反应,其电极反应式是O2+2H2O+4e-=4OH-.

(3)该小组对图2甲中0-t1时压强变大的原因提出了如下假设,请你完成假设二::
假设一:发生析氢腐蚀产生了气体;
假设二:反应放热使锥形瓶内温度升高;
(4)为验证假设一,某同学设计了检验收集的气体中是否含有H2的方案,请你再设计一个实验方案验证假设一.
(1)请完成以下实验设计表(表中不要留空格):
| 编号 | 实验目的 | 碳粉/g | 铁粉/g | 醋酸/% |
| ① | 为以下实验作参照 | 0.5 | 2.0 | 90.0 |
| ② | 0.5 | 2.0 | 36.0 | |
| ③ | 碳粉质量的影响 | 0.2 | 90.0 |

(3)该小组对图2甲中0-t1时压强变大的原因提出了如下假设,请你完成假设二::
假设一:发生析氢腐蚀产生了气体;
假设二:反应放热使锥形瓶内温度升高;
(4)为验证假设一,某同学设计了检验收集的气体中是否含有H2的方案,请你再设计一个实验方案验证假设一.
14.X和Y是短周期元素,两者能组成化合物X2Y3,已知X的原子序数为n,则Y的原子序数不可能是( )
| A. | n+11 | B. | n-5 | C. | n+3 | D. | n+5 |
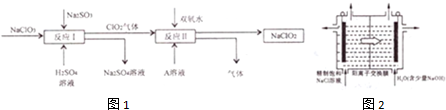
 ?+3nO2$\stackrel{点燃}{→}$2nCO2+2nH2O.
?+3nO2$\stackrel{点燃}{→}$2nCO2+2nH2O.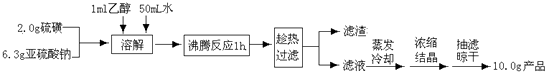

 HClO2+OH-(用离子方程式表示).
HClO2+OH-(用离子方程式表示).