题目内容
17.下列说法不正确的是( )| A. | 能量的释放或吸收是以发生变化的物质为基础的,二者密不可分,但以物质为主,如果物质没有变化,就不能引发能量的变化 | |
| B. | 氢能的优点是燃烧热值高,资源丰富,无毒无污染,且便于储存和运输,因此很可能成为未来的主要能源 | |
| C. | 对于在给定条件下反应物之间能够同时发生多个反应的情况,理想的催化剂还可以大幅度提高目标产物在最终产物中的比率 | |
| D. | 离子反应的速率决定于溶液中离子的浓度和离子的扩散速率,受温度影响不大,是一类不需要活化能来引发的反应,所以反应速率很高 |
分析 A.物质的三态变化有能量变化;
B.氢气是一种新能源.氢气热值高,水作为其原料,资源实在太丰富了,氢气燃烧产物为水无污染;
C.催化剂具有选择性;
D.影响反应因素中温度对反应速率影响大,依据阿伦尼乌斯公式分析,化学反应的活化能越大,温度对化学反应速率的影响越大.
解答 解:A.物质的三态变化有能量变化,物质没有变化,故A错误;
B.氢气是一种新能源.氢气热值高,水作为其原料,资源实在太丰富了,氢气燃烧产物为水无污染,很可能成为未来的主要能源,故B正确;
C.催化剂只能对主反应即生成目标产物的那个反应起起作用,这样在转化率一定的时候的确目标产物的比例会加大,并不是催化剂对所有反应都能同等程度促进,故C错误;
D.离子反应的活化能较小,依据阿伦尼乌斯公式分析,化学反应的活化能越小,温度对化学反应速率的影响越小,反应速率受温度的影响不大,故D错误.
故选B.
点评 本题考查较为综合,多角度考查化学反应与能量、氢能、催化剂以及活化能等知识,侧重于化学与生活、生产、环境的考查,有利于培养学生的良好的科学素养,难度不大.

练习册系列答案
相关题目
7.下列化学用语表达正确的是( )
| A. | CO2分子比例模型: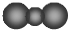 | |
| B. | 氨基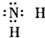 | |
| C. | 原子结构示意图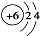 表示12C,也可以表示14C 表示12C,也可以表示14C | |
| D. | 乙炔的最简式 CH≡CH |
8.下列化学用语正确的是( )
| A. | 甲烷的球棍模型: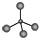 | B. | 羟基的电子式: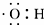 | ||
| C. | 乙醛的结构式:CH3CHO | D. | 乙酸的结构简式C2H4O2 |
5.把金属钠投入下列溶液中,反应后溶液质量减轻的是( )
| A. | HCl | B. | Na2SO4 | C. | NaCl | D. | CuSO4 |
12.NO是一种性质活泼的大气污染物,它能与很多物质发生反应.
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?(g)体系中,n(NO)随时间的变化如表:
(1)写出该反应的平衡常数表达式:K=$\frac{{c}^{2}(N{O}_{2})}{{c}^{2}(NO)•c({O}_{2})}$.已知K300°C >K350°C,则该反应是放热反应.
(2)图中表示NO2的变化的曲线是b.用O2表示从0-2 s内该反应的平均速率v=0.0015mol/(L•s).
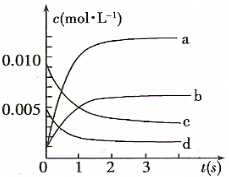
(3)为使该反应的反应速率增大,且平衡向正反应方向移动的是c.
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度d.选择高效催化剂.
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?(g)体系中,n(NO)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.01. | 0.008 | 0.007 | 0.007 | 0.007 |
(2)图中表示NO2的变化的曲线是b.用O2表示从0-2 s内该反应的平均速率v=0.0015mol/(L•s).

(3)为使该反应的反应速率增大,且平衡向正反应方向移动的是c.
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度d.选择高效催化剂.
2.设NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 2.4g镁变为镁离子失去的电子数为0.1NA | |
| B. | 电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量减少64g | |
| C. | 标准状况下,2.24L四氯化碳含有分子的数目为0.1NA | |
| D. | 常温常压下,Na2O2与足量H2O反应,当生成0.2molO2时,转移电子的数目为0.4NA |
 常见金属X,有下列关系图,根据图示回答:
常见金属X,有下列关系图,根据图示回答: