题目内容
5.把金属钠投入下列溶液中,反应后溶液质量减轻的是( )| A. | HCl | B. | Na2SO4 | C. | NaCl | D. | CuSO4 |
分析 钠和水反应生成氢氧化钠和氢气,会出现气体,如果溶液质量减轻,则说明从溶液中放出气体的质量大于溶液增加的质量,根据金属钠和下列物质间的反应情况来解答.
解答 解:A.钠和盐酸的反应方程式为:2Na+2HCl═2NaCl+H2↑,根据方程式知,溶液增加的质量=m(Na)-m(H2),溶液质量增加,故A错误;
B.将金属钠加入到硫酸钠溶液中,只有金属钠和水之间反应,钠和水的反应方程式为:2Na+2H2O═2NaOH+H2↑,根据方程式知,溶液增加的质量=m(Na)-m(H2),溶液质量增加,故B错误;
C.将金属钠加入到氯化钠溶液中,只有金属钠和水之间反应,钠和水的反应方程式为:2Na+2H2O═2NaOH+H2↑,根据方程式知,溶液增加的质量=m(Na)-m(H2),溶液质量增加,故C错误;
D.钠和水的反应方程式为:2Na+2H2O═2NaOH+H2↑,生成的氢氧化钠和硫酸铜反应,方程式为:2NaOH+CuSO4═Na2SO4+Cu(OH)2↓,将两个方程式相加:2Na+2H2O+CuSO4═H2↑+Na2SO4+Cu(OH)2↓,由方程式知,溶液的质量减轻,故D正确;
故选:D.
点评 本题考查了元素化合物知识,熟悉钠的性质是解题关键,注意钠与盐溶液反应实质是先与水反应,依据差量法不难解答.

练习册系列答案
相关题目
13.2011年3月,双汇“瘦肉精”事件爆发,目前由于奸商的违法经营,已使“瘦肉精”变成了“害人精”.“瘦肉精”的结构可表示为: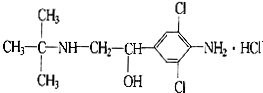 下列关于“瘦肉精”的说法中正确的是( )
下列关于“瘦肉精”的说法中正确的是( )
 下列关于“瘦肉精”的说法中正确的是( )
下列关于“瘦肉精”的说法中正确的是( )| A. | 摩尔质量为305.5 | |
| B. | 属于芳香族化合物,也是高分子化合物 | |
| C. | 1mol该有机物在一定条件下可与3 mol氢气发生加成反应 | |
| D. | 向此有机物中加入硝酸酸化的硝酸银溶液会产生淡黄色的沉淀 |
20.配制250mL0.10mol•L-1的NaOH溶液时,下列实验操作会使配得的溶液浓度偏大的是( )
| A. | 转移溶液后未洗涤烧杯和玻璃棒就直接定容 | |
| B. | 所用NaOH已经潮解 | |
| C. | 带游码的天平称2.4gNaOH时误用了“左码右物”方法 | |
| D. | 在容量瓶中进行定容时俯视刻度线 |
10.下列物质的水溶液中不存在溶质分子的是( )
| A. | H2S | B. | HF | C. | HNO3 | D. | NH3•H2O |
17.下列说法不正确的是( )
| A. | 能量的释放或吸收是以发生变化的物质为基础的,二者密不可分,但以物质为主,如果物质没有变化,就不能引发能量的变化 | |
| B. | 氢能的优点是燃烧热值高,资源丰富,无毒无污染,且便于储存和运输,因此很可能成为未来的主要能源 | |
| C. | 对于在给定条件下反应物之间能够同时发生多个反应的情况,理想的催化剂还可以大幅度提高目标产物在最终产物中的比率 | |
| D. | 离子反应的速率决定于溶液中离子的浓度和离子的扩散速率,受温度影响不大,是一类不需要活化能来引发的反应,所以反应速率很高 |
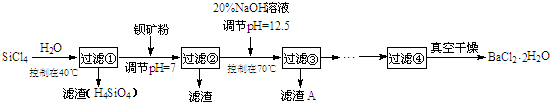
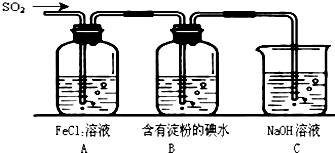 某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示: