��Ŀ����
����Ŀ�����������ָ�ܽ�̫����ֱ��ת���ɵ��ܵIJ��ϡ���������ֳ�̫���ܲ��ϣ�ֻ�а뵼����Ͼ������ֹ��ܡ�����̫����ز��ϵ��е����衢�ྦྷ�衢�Ǿ��衢GaAs��GaAlAs��InP��CdS��CdTe��CuInSe�ȡ�
��1����֪Se�����ڱ���λ��Ϊ_____����Ļ�̬ԭ�ӵ����Ų�ʽΪ_____,��̬Gaԭ�Ӻ������ռ�ݵ�����ܼ�Ϊ_____��ͭ�Ļ�̬ԭ�Ӽ۵����Ų�ͼΪ_____��
��2��P��S��Ga�縺�ԴӴ�С��˳��Ϊ_____��
��3����AlԪ�ش���ͬһ�������Ԫ�ؾ���ȱ�����ԣ��仯�����������мӺ��ԣ��������(H3BO3)��ˮ��Һ������ˮ��Ӧ����[B(OH)4]-������һԪ��������ʣ�[B(OH)4]-�ĽṹʽΪ____�������λ����
��4����֪[Cu(H2O)4]2+���жԳƵĿռ乹�ͣ�[Cu(H2O)4]2+�е�2��H2O��Cl-ȡ�����ܵõ�2�ֲ�ͬ�ṹ�IJ����[Cu(H2O)4]2+�Ŀռ乹��Ϊ_____��
��5��AsԪ�صĵ�һ������____SeԪ�صĵ�һ������(����ڡ�����С�ڡ����ڡ�)��ԭ����__________��
��6��̫����ز��ϵĺܶ���������������������ʱ���������Ļ�����ɫ������ԭ�ӽṹ��֪ʶ���������������ԭ����____��
���𰸡���������VIA�� 1s22s22p63s23p2����[Ne]3s23p2 4p 3d104s1 S��P��Ga 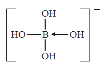 ƽ���ı��� ���� �� ��
ƽ���ı��� ���� �� ��
��������
��1��Se��34��Ԫ�أ�4�����Ӳ㡢�����6�����ӣ��������14�����ӣ������������ԭ����д��ԭ�Ӻ�������Ų�ʽ�������������ԭ����������Ӵӵ��ܼ�����ܼ��Ų��������������ԭ�������ع������ͭ�Ļ�̬ԭ�Ӽ۵����Ų�ͼ��
��2��ͬ����Ԫ�ش����ҵ縺��������ͬ����Ԫ�ش��ϵ��µ縺�Լ�С��
��3��H3BO3��ˮ��Ӧ����[B(OH)4]-ʱ�γ�1����λ����
��4��[Cu��NH3��4]2+���жԳƵĿռ乹�ͣ������Ϊ��������ṹ��ƽ�������νṹ��ƽ�������νṹ�����ֲ�ͬ�Ķ��ȴ����������ṹ��һ�ֶ��ȴ��
��5���顢�����ǵ�4���ڷǽ���Ԫ�أ�ͬһ����Ԫ��������ҵ�һ�����ܳ��������ƣ�����Ԫ��ԭ��4p�ܼ��ǰ����ȶ�״̬�������ϵͣ���һ�����ܸ���ͬ��������Ԫ�أ�
��6������̬ԭ�ӵĵ��������������ӻ�ԾǨ���ϸ��ܼ�����ɼ���̬ԭ�ӣ����Ӵӽϸ������ļ���̬ԾǨ���ϵ������ļ���̬������̬ʱ�����Թ����ʽ�ͷ�������
��1��Se��34��Ԫ�أ�4�����Ӳ㡢�����6�����ӣ������ڱ���λ��Ϊ��������VIA�壻�������14�����ӣ������������ԭ������ԭ�Ӻ�������Ų�ʽ��1s22s22p63s23p2�� Ga��31��Ԫ�أ�������31�����ӣ���̬Gaԭ�ӵ����Ų�ʽΪ1s22s22p63s23p63d104s24p1������ܼ�Ϊ4p�������������ԭ�������ع���ͭ�Ļ�̬ԭ�Ӽ۵����Ų�ͼ��3d104s1��
��2��ͬ����Ԫ�ش����ҵ縺��������ͬ����Ԫ�ش��ϵ��µ縺�Լ�С�����Ե縺��S��P��Ga��
��3��H3BO3��ˮ��Ӧ����[B(OH)4]-ʱ�γ�1����λ����[B(OH)4]-�ĽṹʽΪ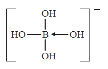 ��
��
��4��[Cu��NH3��4]2+���жԳƵĿռ乹�ͣ������Ϊ��������ṹ��ƽ�������νṹ��ƽ�������νṹ�����ֲ�ͬ�Ķ��ȴ����������ṹ��һ�ֶ��ȴ��[Cu(H2O)4]2+�е�2��H2O��Cl-ȡ�����ܵõ�2�ֲ�ͬ�ṹ�IJ����[Cu(H2O)4]2+�Ŀռ乹��Ϊƽ���ı��Σ�
��5���顢�����ǵ�4���ڷǽ���Ԫ�أ�ͬһ����Ԫ��������ҵ�һ�����ܳ��������ƣ�����Ԫ��ԭ��4p�ܼ��ǰ����ȶ�״̬�������ϵͣ���һ�����ܸ���ͬ��������Ԫ�أ�����AsԪ�صĵ�һ�����ܴ���SeԪ�صĵ�һ�����ܣ�
��6������̬ԭ�ӵĵ��������������ӻ�ԾǨ���ϸ��ܼ�����ɼ���̬ԭ�ӣ����Ӵӽϸ������ļ���̬ԾǨ���ϵ������ļ���̬������̬ʱ�����Թ����ʽ�ͷ���������������Ļ�����ɫ��

 ����С״Ԫ��������������ϵ�д�
����С״Ԫ��������������ϵ�д� ����������ϵ�д�
����������ϵ�д�����Ŀ��NF3�������������ڳ��³�ѹ������ɫ����ζ�����壬�����ӹ�ҵ��һ�������ĵ�����ʴ�����塣�ش��������⣺
��1��NF3�ĵ���ʽΪ______��NԪ�صĻ��ϼ�Ϊ______��
��2��F2��NH3ֱ�ӷ�Ӧ����NF3�Ļ�ѧ����ʽΪ______��
��3��ʵ����ģ�ҵ�����õ������NH4HF2��NH4FHF������ȡNF3������Ϊ��NiΪ�������ϵĺϽ��ں����������������������������ķ�Ӧ��������Ϊ̼�ظ֣�����Һ�ɻ��������á�
�ٵ��ʱNF3��______�����ɣ�����������������______���ѧʽ����
�ڵ����Һ����Ni����Fe��Cu�ĵ��ʼ�NH4HF2�ȣ��ɾ��������̽��л��������ã�
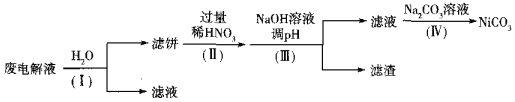
��֪��ʵ�������£����ֽ������ӿ�ʼ�����������ȫ��pH���±�
�������� | Ni2+ | Fe2+ | Cu2+ | Fe3+ |
��ʼ����ʱ��pH | 7.2 | 7.0 | 4.7 | 1.9 |
������ȫʱ��pH | 9.2 | 9.0 | 6.7 | 3.2 |
����I��Ŀ����______��������˱���Ni������������ӷ���ʽΪ______��HNO3�Ļ�ԭ����ΪNO������������pHʱ��������pHӦ���Ƶķ�Χ��______��