题目内容
【题目】已知下列两个热化学方程式:2H2(g) + O2(g) = 2H2O(1) ΔH= -571.6 kJmol-1,C3H8(g) + 5O2(g)= 3CO2(g) + 4H2O(l) ΔH= -2220 kJmol-1,下列说法正确的是( )
A.相同质量H2和C3H8分别完全燃烧,C3H8放出的热量多
B.C3H8 完全燃烧生成1mol H2O(l)放出的热量为555 kJ
C.l mol H2和2 molC3H8 组成的混合气体完全燃烧放出的热量为5011.6 kJ
D.H2和C3H8的混合气体共4mol,完全燃烧时放出3256 kJ热量,则 n(H2):n(C3H8)=1:1
【答案】B
【解析】
A.相同质量H2和C3H8分别完全燃烧,H2放出的热量多,A不正确;
B.C3H8 完全燃烧生成1mol H2O(l)放出的热量为![]() kJ=555 kJ,B正确;
kJ=555 kJ,B正确;
C.l mol H2和2 molC3H8 组成的混合气体完全燃烧放出的热量为(![]() +2×2220) kJ=4725.8 kJ,C不正确;
+2×2220) kJ=4725.8 kJ,C不正确;
D.H2和C3H8的混合气体共4mol,若n(H2):n(C3H8)=1:1,则完全燃烧时放热一定大于3256 kJ,D不正确;
故选B。

 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案【题目】某化学课外活动小组为了验证元素化学性质递变规律,进行如下实验探究。
Ⅰ![]() 探究1:验证同周期X、Y、Z三种元素金属性递变规律
探究1:验证同周期X、Y、Z三种元素金属性递变规律
实验内容 | 实验现象 |
1、各取1.0g金属X和金属Z,分别加入到5mL水中 | 金属X与水反应比金属Y剧烈 |
2、各取1.0g的金属Z和金属Y形状相同,分别加入到5mL 1.0mol/L盐酸中。 | 金属Y与盐酸反应比金属Z剧烈 |
(1)通过实验验证三种元素金属性由强到弱是_______________________,
(2)下列判断正确的是______
A.原子序数:![]()
![]() 原子的最外层电子数
原子的最外层电子数![]()
C.原子半径:X>Y>Z D. Z的最高价氧化物对应水化物的碱性最强
Ⅱ![]() 探究2:验证氯元素的非金属性比硫元素的非金属性强,设计如下实验:
探究2:验证氯元素的非金属性比硫元素的非金属性强,设计如下实验:
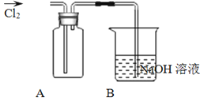
![]() 装置A中盛放的试剂是______
装置A中盛放的试剂是______![]() 填选项
填选项![]()
A.![]() 溶液
溶液![]() 溶液
溶液![]() 溶液
溶液
B中反应的离子方程式是__________________________________________________。
![]() 下列不能用于验证氯元素比硫元素非金属性强的依据为______
下列不能用于验证氯元素比硫元素非金属性强的依据为______![]() 填选项
填选项![]()
A.HCl酸性比![]() 强 B.HClO氧化性比
强 B.HClO氧化性比![]() 强
强
C.HClO3酸性比![]() 强 D.铁与
强 D.铁与![]() 反应生成
反应生成![]() ,而硫与铁反应生成FeS
,而硫与铁反应生成FeS
![]() 若要验证非金属性:
若要验证非金属性:![]() ,装置A中加入淀粉碘化钾混合溶液,观察到装置A中溶液______的现象,即可证明。用原子结构理论解释非金属性
,装置A中加入淀粉碘化钾混合溶液,观察到装置A中溶液______的现象,即可证明。用原子结构理论解释非金属性![]() 的原因:同主族元素从上到下,____________________。
的原因:同主族元素从上到下,____________________。
