题目内容
17.W、X、Y、Z均为短周期元素,W、X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构,W和Z的最外层电子数相同.下列说法正确的是( )| A. | W、X的最高价氧化物对应水化物的酸性:X>W | |
| B. | 单质沸点:Y>Z>W | |
| C. | 离子半径:X->W->Y+>Z- | |
| D. | 结合质子能力:X2->W- |
分析 X、Z的最低价离子分别为X2-和Z-,则X为第ⅥA族元素,Z为ⅦA族元素;Y+和Z-具有相同的电子层结构,则Y在Z的下一周期,则Y为Na元素,Z为F元素,W和Z的最外层电子数相同,W、X、Y同周期,则X为S元素,W为Cl,结合元素在周期表中的位置以及元素周期律知识解答该题.
解答 解:X、Z的最低价离子分别为X2-和Z-,则X为第ⅥA族元素,Z为ⅦA族元素;Y+和Z-具有相同的电子层结构,则Y在Z的下一周期,则Y为Na元素,Z为F元素,W和Z的最外层电子数相同,W、X、Y同周期,则X为S元素,W为Cl,
A.非金属性Cl>S,则W、X的最高价氧化物对应水化物的酸性:X<W,故A错误;
B.由分子构成的物质相对分子质量越大沸点越大,且常温下Na为固体,则单质沸点:Y>W>X,故B错误;
C.Na+、F-具有相同的核外电子排布,离子的核电荷数越大,半径越小,应为F->Na+,S2-和Cl-具有相同电子排布,离子半径为S2->Cl-,且电子层越多,离子半径越大,则离子半径为X->W->Z->Y+,故C错误;
D.S、Cl对应氢化物的酸性越强,结合质子能力越弱,HCl为强酸,则结合质子能力为X2->W-,故D正确;
故选D.
点评 本题考查原子结构与元素周期律的关系,为高考常见题型,侧重于学生的分析能力的考查,本题的关键是根据原子结构特点正确推断元素的种类,题目难度不大.

练习册系列答案
相关题目
7.下列叙述中正确的是( )
| A. | 氧化剂中的每一种元素在反应中都得到电子 | |
| B. | 还原剂在同一反应中既可以是反应物,也可以是生成物 | |
| C. | 失电子多的还原剂,还原性不一定强 | |
| D. | 阳离子只有氧化性,阴离子只有还原性 |
8.下列说法不正确的是( )
| A. | (CH3)2C=CHCH2CH3的名称为2-甲基-2-戊烯 | |
| B. | 乙醇、乙二醇、丙三醇的沸点依次升高 | |
| C. | 1mol乙酰水杨酸( 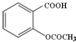 )最多可以和2mol NaOH反应 )最多可以和2mol NaOH反应 | |
| D. | 可用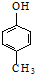 和HCHO 为原料合成 和HCHO 为原料合成 |
5.现有0.1mol•L-1的醋酸溶液,下列说法正确的是( )
| A. | 加水稀释,溶液中所有离子的浓度都减小 | |
| B. | 溶液中n(CH3COO-)+n(CH3COOH)=0.1mol | |
| C. | 升高温度,醋酸的电离度增大 | |
| D. | 中和1L等物质的量浓度的NaOH溶液所消耗的醋酸体积大于1L |
2.关于下列各实验装置的叙述中,不正确的是( )
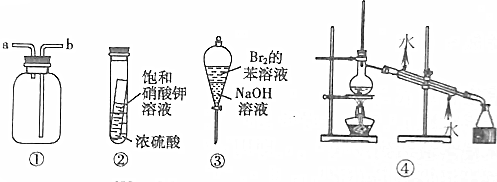

| A. | 装置①可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体 | |
| B. | 实验②放置一段时间后,小试管内有晶体析出 | |
| C. | 实验③振荡后静置,上层溶液颜色变浅 | |
| D. | 实验④可用于分离饱和Na2CO3溶液和CH3COOC2H5 |