题目内容
14.可逆反应 2A(s)+3B(g)?C(g)+2D(g)△H<0,在一定条件下达到平衡,下列有关叙述正确的是( )| A. | 增加A的量,B的转化率提高 | |
| B. | 压强增大平衡不移动,v(正)、v(逆)均不变 | |
| C. | 增大B的浓度,v(正)>v(逆) | |
| D. | 升高温度,平衡向逆反应方向移动,v(正)减小 |
分析 A、A是固体,其量的变化对平衡无影响;
B、压强增大平衡不移动,但v(正)、v(逆)都增大;
C、增大B的浓度,平衡向正反应移动;
D、升高温度,正、逆反应速率都增大.
解答 解:A、A是固体,增大A的量对平衡无影响,故A错误;
B、压强增大平衡不移动,但v(正)、v(逆)都增大,故B错误;
C、增大B的浓度,反应速率增大,平衡向正反应方向移动,v(正)>v(逆),故C正确;
D、升高温度,v(正)、v(逆)均应增大,但v(逆)增大的程度大,平衡向逆反应方向移动,故D错误;
故选C.
点评 本题考查化学平衡的影响因素,比较基础,注意化学平衡发生移动的本质是改变条件引起正、逆速率不相等.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
5.某芳香族酯类化合物甲的分子式为C14H10O5,1mol甲水解后只生成一种产物乙,其物质的量为2mol,下列说法正确的是( )
| A. | 符合上述条件的甲共有3种 | |
| B. | 1mol甲最多可以和7molH2发生反应 | |
| C. | 乙中的所有原子一定共平面 | |
| D. | 分别燃烧1mol乙与1mol苯耗氧量相同 |
2.化学式为C7H16的烷烃中,在结构式中含有3个甲基的同分异构体数目是( )
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
9.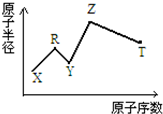 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )
 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )| A. | 原子半径和离子半径均满足:Y<Z | |
| B. | 氢化物的沸点排序:Y>T>R | |
| C. | 最高价氧化物对应的水化物的酸性:T<R | |
| D. | 由X、R、Y、Z四种元素组成的化合物水溶液一定显酸性 |
6.能说明氯元素的非金属性比硫元素强的事实是( )
| A. | HCl比H2S稳定 | B. | 常温下Cl2为气体,S单质为固体 | ||
| C. | 单质S可以在空气中燃烧Cl2不能 | D. | 溶于水时HCl是强酸而H2S是弱酸 |
4.在钢铁的生锈过程中(吸氧腐蚀)可能发生的反应是( )
| A. | 4Fe+3O2═2Fe2O3 | B. | O2+4e-+2H2O═4OH- | ||
| C. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | D. | Fe+2H+═Fe2++H2↑ |