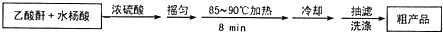题目内容
4.在钢铁的生锈过程中(吸氧腐蚀)可能发生的反应是( )| A. | 4Fe+3O2═2Fe2O3 | B. | O2+4e-+2H2O═4OH- | ||
| C. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | D. | Fe+2H+═Fe2++H2↑ |
分析 当电解质溶液为中性或弱酸性时,钢铁会发生吸氧腐蚀,铁在负极放电,氧气在正极放电,根据电极反应式来分析.
解答 解:当电解质溶液为中性或弱酸性时,钢铁会发生吸氧腐蚀,铁在负极放电:Fe-2e-=Fe2+,氧气在正极放电:O2+4e-+2H2O=4OH-,故得总反应:2Fe+O2+2H2O=2Fe(OH)2,而Fe(OH)2有强氧化性,易被氧气氧化:4Fe(OH)2+O2+2H2O=4Fe(OH)3,Fe(OH)3又会分解:2Fe(OH)3=Fe2O3•xH2O+(3-x)H2O,故选BC.
点评 本题考查了钢铁的吸氧腐蚀的两极反应和总反应,难度不大,掌握基础是解题关键.

练习册系列答案
相关题目
14.可逆反应 2A(s)+3B(g)?C(g)+2D(g)△H<0,在一定条件下达到平衡,下列有关叙述正确的是( )
| A. | 增加A的量,B的转化率提高 | |
| B. | 压强增大平衡不移动,v(正)、v(逆)均不变 | |
| C. | 增大B的浓度,v(正)>v(逆) | |
| D. | 升高温度,平衡向逆反应方向移动,v(正)减小 |
15.据科学家预测,月球的土壤中吸附着数百万吨的${\;}_{2}^{3}$He,每百吨${\;}_{2}^{3}$He核聚变所释放出的能量相当于目前人类一年消耗的能量.在地球上氦元素主要以${\;}_{2}^{4}$He的形式存在.下列说法正确的是( )
| A. | ${\;}_{2}^{4}$He原子核内含有4个质子 | B. | ${\;}_{2}^{3}$He原子核内含有3个中子 | ||
| C. | ${\;}_{2}^{3}$He和${\;}_{2}^{4}$He互为同位素 | D. | ${\;}_{2}^{3}$He和${\;}_{2}^{4}$He互为同素异形体 |
12.下列说法正确的是( )
| A. | 离子化合物只能由金属元素和非金属元素组成 | |
| B. | 离子化合物只能存在离子键 | |
| C. | HCl能电离出氢离子和氯离子,所以HCl存在离子键 | |
| D. | 共价化合物中不可能存在离子键 |
19.下列各组物质中,互称为同分异构体的是( )
| A. | 水与冰 | B. | CH4和CH3CH3 | C. | 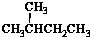 与 与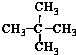 | D. | 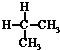 与 与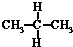 |
9.准确配制一定物质的量浓度的NaOH溶液,下面实验操作中不正确的是( )
| A. | 用托盘天平称量时,应将NaOH固体放在小烧杯或玻璃器皿中 | |
| B. | 将烧杯中未冷却的NaOH溶液直接注入未经干燥的容量瓶中 | |
| C. | 定容时视线应平视凹液面(或平视刻度线),直到凹液面的最低点与刻度线相切 | |
| D. | 将称好的NaOH固体放入烧杯中,加入适量水溶解 |
7.下表是A、B、C、D四种有机物的有关信息.
请回答下列问题.
(1)写出有机物C的结构简式HCOOH.
(2)写出B→D的化学反应方程式CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2↑+H2O.
(3)写出A与NH3在一定条件下反应生成丙烯酰胺的化学方程式,并指出反应类型:CH2=CHCOOH+NH3→CH2=CHCOONH2+H2O,反应类型取代反应.
(4)丙烯酰胺有多种同分异构体,试写出分子中同时含有醛基和碳碳双键的3种同分异构体的结构简式CH2=CHNHCHO、CH2=C(NH2)CHO、CH(NH2)=CHCHO.
| A | 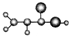 ①由C、H、O三种元素组成 ②球棍模型为: ③能与NH3在一定条件下反应生成丙烯酰胺CH2=CHCONH2 ④相对分子质量为72 |
| B | ①由C、H、O三种元素组成 ②能与Na反应,但不能与NaOH溶液反应 ③能与A反应生成相对分子质量为100的酯 |
| C | ①相对分子质量与B相同 ②能被新制的氢氧化铜悬浊液氧化 ③能与NaHCO3溶液反应放出CO2气体 |
| D | ①能使溴的四氯化碳溶液褪色 ②能与水在一定条件下反应生成B |
(1)写出有机物C的结构简式HCOOH.
(2)写出B→D的化学反应方程式CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2↑+H2O.
(3)写出A与NH3在一定条件下反应生成丙烯酰胺的化学方程式,并指出反应类型:CH2=CHCOOH+NH3→CH2=CHCOONH2+H2O,反应类型取代反应.
(4)丙烯酰胺有多种同分异构体,试写出分子中同时含有醛基和碳碳双键的3种同分异构体的结构简式CH2=CHNHCHO、CH2=C(NH2)CHO、CH(NH2)=CHCHO.
 阿司匹林(又称乙酰水杨酸,
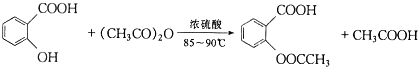
阿司匹林(又称乙酰水杨酸, 是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128-135℃.某学习小组在实驻室以水杨酸(邻羟基苯甲酸)与乙酸酐[(CH3CO)2O]为主要原料合成阿司匹林,其制备原理为:
是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128-135℃.某学习小组在实驻室以水杨酸(邻羟基苯甲酸)与乙酸酐[(CH3CO)2O]为主要原料合成阿司匹林,其制备原理为: