题目内容
18.为了证明甲酸溶液中含有少量甲醛,正确的实验操作是( )| A. | 加入银氨溶液,在水浴上加热 | |
| B. | 加入二至三滴紫色石蕊试液 | |
| C. | 先蒸馏,然后对蒸出的物质的水溶液进行银镜反应实验 | |
| D. | 先加入足量的NaOH溶液,然后蒸馏,对蒸出的物质的水溶液进行银镜反应实验 |
分析 A.银镜反应需要在碱性环境下发生;
B.石蕊试液只能检验溶液的酸碱性,不能检验甲醛的存在;
C.甲醛少量,蒸馏难以分离出甲醛;
D.利用甲醛能够发生银镜反应的性质解答.
解答 解:A.为了证明甲酸溶液中含有少量甲醛,应先加入过量氢氧化钠使溶液呈碱性,再进行银镜反应,故A错误;
B.石蕊试液只能检验溶液的酸碱性,不能检验甲醛的存在,故B错误;
C.甲醛少量,蒸馏难以分离出甲醛,故C错误;
D.甲醛在碱性环境下能够与银氨溶液发生银镜反应,故D正确;
故选:D.
点评 本题考查了醛基的检验,明确银镜反应发生的条件是解题关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.下列物质中含有既有离子键又有共价键的是( )
| A. | 氯化氢 | B. | 乙醇 | C. | 碘 | D. | 氢氧化钠 |
10.将浓硝酸分解的气体收集在一支试管中,再将试管倒插在水中,可能出现的现象是试管内液面上升,原因是:NO2和O2的混合气体溶于水使试管内压强减小,化学方程式为4NO2+O2+2H2O=4HNO3 .
16.为了回收利用SO2,研究人员研制了利用低品位软锰矿浆(主要成分是MnO2)吸收高温焙烧含硫废渣产生的SO2废气,制备硫酸锰晶体的生产流程,其流程示意图如下:
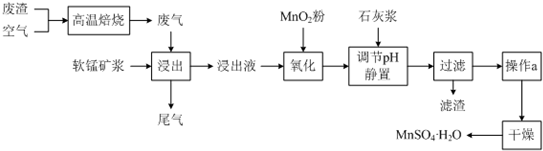
已知,浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子.有关金属离子形成氢氧化物沉淀时的pH见下表:
请回答下列问题:
(1)写出浸出过程中主要反应的化学方程式:SO2+MnO2=MnSO4.
(2)写出氧化过程中主要反应的离子方程式:2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
(3)在氧化后的液体中加入石灰浆,并用pH试纸测定调节pH,pH应调节范围是4.7~8.3.

已知,浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子.有关金属离子形成氢氧化物沉淀时的pH见下表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
(1)写出浸出过程中主要反应的化学方程式:SO2+MnO2=MnSO4.
(2)写出氧化过程中主要反应的离子方程式:2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
(3)在氧化后的液体中加入石灰浆,并用pH试纸测定调节pH,pH应调节范围是4.7~8.3.
17.25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.1 mol•L-1pH=4的NaHA溶液中:c(Na+)=c(HA-)+2c(A2-) | |
| B. | 在0.1 mol•L-1Na2CO3溶液中:c(OH-)+c(H+)=c(HCO3-)+2c(H2CO3) | |
| C. | pH相等的①CH3COONa ②NaHCO3 ③NaClO三种溶液的c(Na+):①>②>③ | |
| D. | NH3•H2O和NH4Cl的混合溶液[pH=7,c(Cl-)=0.1 mol•L-1]:c(NH4+)>c(Cl-)>c(H+)=c(OH-) |
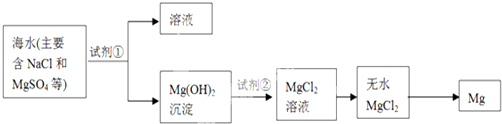
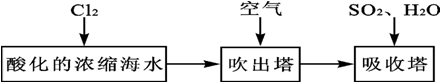
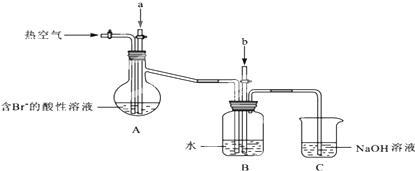
 到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.
到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.