题目内容
17.下列有关说法正确的是( )| A. | 白铁(镀锌铁皮)镀层破损后铁仍不易腐蚀 | |
| B. | CH3Cl(g)+Cl2(g)$\stackrel{光照}{→}$CH2Cl2(l)+HCl(g)能自发进行,则该反应的△H>0 | |
| C. | MnS悬浊液中滴加少量CuSO4溶液可生成CuS沉淀,则Ksp(CuS)<Ksp(MnS) | |
| D. | 合成氨生产中将NH3液化分离,一定能加快正反应速率,提高H2的转化率 |
分析 A、在金属活动性顺序表中锌比铁活泼,所以破损后仍腐蚀的是锌,保护的是铁;
B、CH3Cl(g)+Cl2(g)$\stackrel{光照}{→}$CH2Cl2(l)+HCl(g)为气体减少的反应所以△S<0,根据△G=△H-T△S<0自发判断;
C、Ksp反映物质的溶解程度,沉淀向着Ksp更小的物质转化;
D、减小生成物的浓度会使得平衡正向移动,减小反应的速率.
解答 解:A、在金属活动性顺序表中锌比铁活泼,所以破损后仍腐蚀的是锌,保护的是铁,能用金属活动性顺序表解释,故A正确;
B、CH3Cl(g)+Cl2(g)$\stackrel{光照}{→}$CH2Cl2(l)+HCl(g)为气体减少的反应所以△S<0,又△G=△H-T△S<0才自发,所以只有当△H<0反应才可能自发,故B错误;
C、沉淀向着Ksp更小的物质转化,当MnS悬浊液中滴加少量CuSO4溶液可生成CuS沉淀,则Ksp(CuS)<Ksp(MnS),故C正确;
D、合成氨生产中将NH3液化分离,降低正反应速率,提高H2的转化率,故D错误.
故选AC.
点评 本题涉及金属的腐蚀和防护、化学反应的方向、速率和平衡以及沉淀的转化等知识,属于综合知识的考查,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.化合物M是从微生物中分离得到的,它显示出广谱抗菌活性.下列关于化合物M的说法中错误的是( )


| A. | 化合物M的分子式为C14H15NO7 | |
| B. | 化合物M能使酸性KMnO4溶液褪色 | |
| C. | 化合物M能发生加成反应,不能发生消去反应 | |
| D. | 1mol在NaOH溶液中反应,最多消耗4molNaOH |
5.化学与生活、环境密切相关,下列说法正确的是( )
| A. | 氢氧化钠和氢氧化铝都可治疗胃酸过多 | |
| B. | 葡萄酒中常含有一定量的S02用来防氧化和杀菌 | |
| C. | 酱油中含有三价铁可补充人体缺乏的铁元素 | |
| D. | 石油分馏的目的是为了获得乙烯、丙烯和丁二烯 |
2.如图所示,常温时将一滴管液体Y一次性全部挤到充满O2的锥形瓶内(装置气密性良好),若锥形瓶内气体的最大物质的量是amol,久置后其气体的物质的量是bmol,不存在a>b关系的是( )
| X | Y | 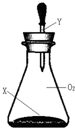 | |
| A | 过量C、Fe碎屑 | 稀HCl | |
| B | 过量Na2CO3粉末 | 稀H2SO4 | |
| C | 过量Fe、Al碎屑 | 浓H2SO4 | |
| D | 过量Cu、CuO粉末 | 浓HNO3 |
| A. | A | B. | B | C. | C | D. | D |
9.用NA表示阿伏加德罗常数,下列说法中正确的有( )
| A. | pH=13的NaOH溶液中含有的OH-的数为0.1 NA | |
| B. | Fe在少量Cl2中燃烧生成0.5 mol 产物,转移的电子数为1 NA | |
| C. | 18g D2O中含有的质子数为9NA | |
| D. | 标准状况下,含4 mol HCl的浓盐酸与足量MnO2加热反应可生成22.4 L氯气 |
6.如图所示是Zn和Cu形成的原电池,说法正确的是( )


| A. | 铜为负极,锌为正极 | B. | 正极反应为Zn-2e-=Zn2+ | ||
| C. | 电子由铜片通过导线流向锌片 | D. | 原电池的反映本质是氧化还原反应 |
7.下列反应产生的气体,在标准状况下体积最大的是( )
| A. | 将1 mol MnO2加入足量浓盐酸中,加热 | |
| B. | 将l mol Na2O2加入足量水中, | |
| C. | 将1 mol Cu加入足量稀硝酸中,加热 | |
| D. | 将1 mol C加入足量浓硫酸中,加热 |
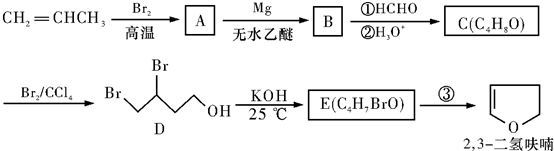
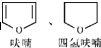
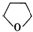 +H2O.
+H2O.