题目内容
8.化合物M是从微生物中分离得到的,它显示出广谱抗菌活性.下列关于化合物M的说法中错误的是( )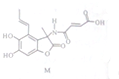
| A. | 化合物M的分子式为C14H15NO7 | |
| B. | 化合物M能使酸性KMnO4溶液褪色 | |
| C. | 化合物M能发生加成反应,不能发生消去反应 | |
| D. | 1mol在NaOH溶液中反应,最多消耗4molNaOH |
分析 由有机物的结构简式可确定有机物的分子式,该有机物中含有酚羟基,可发生取代、氧化和显色反应,含有碳碳双键,可发生加成、加聚和氧化反应,含有肽键和酯基,可发生水解反应,含有羧基,具有酸性,可发生中和和酯化反应,以此解答该题.
解答 解:A.由结构简式该有机物的分子式为C14H15NO7,故A正确;
B.含有酚羟基和碳碳双键,可被酸性高锰酸钾氧化,故B正确;
C.羟基连接在苯环上,不能发生消去反应,含有碳碳双键和苯环,可发生加成反应,故C正确;
D.能与氢氧化钠反应的为酚羟基、酯基和羧基,且酯基水解生成酚羟基,另外肽键水解也能生成羧基,消耗氢氧化钠,则1mol在NaOH溶液中反应,最多消耗6molNaOH,故D错误.
故选D.
点评 本题考查学生有关官能团决定性质的知识与空间结构等,要求学生熟记官能团具有的性质,本题易错点为D,注意把握官能团的性质,根据官能团判断有机物的性质,难度不大.

练习册系列答案
 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
14.关于下列各实验装置图的叙述中,不正确的是( )
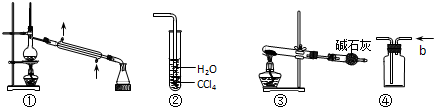

| A. | 装置①常用于分离某些互溶的液体混合物 | |
| B. | 装置②可用于吸收HCl气体,并防止倒吸 | |
| C. | 以NH4HCO3为原料,装置③可用于实验室制备少量NH3 | |
| D. | 装置④b口进气,可用排空气法收集H2、NO等气体 |
11.下列设计的实验方案能达到实验目的是( )
| A. | 制备Al(OH)3悬浊液:向1mol•L-1AlCl3溶液中加过量的6mol•L-1NaOH溶液 | |
| B. | 提纯含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入过量饱和Na2CO3溶液,振荡后静置分液,并除去有机相的水 | |
| C. | 检验溶液中是否含有Fe2+:取少量待检验溶液,向其中加入少量新制氯水,再滴加KSCN溶液,观察实验现象 | |
| D. | 探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL5%H2O2和1mLH2O,向另一支试管中加入2mL5%H2O2和1mLFeCl3溶液,观察并比较实验现象 |
3.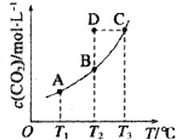 在恒容密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g).CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示.下列说法错误的是 ( )
在恒容密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g).CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示.下列说法错误的是 ( )
 在恒容密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g).CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示.下列说法错误的是 ( )
在恒容密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g).CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示.下列说法错误的是 ( )| A. | 反应CO(g)+H2O(g)?CO2(g)+H2(g)为吸热反应 | |
| B. | 在T2时,若反应处于状态D,则一定有υ正>υ逆 | |
| C. | 平衡状态A 与C 相-比,平衡状态A 的c(CO)大 | |
| D. | 若T1、T2 时的平衡常数分别为K1、K2则K1>K2 |
13.有Br2参加的化学反应一定不属于( )
| A. | 复分解反应 | B. | 置换反应 | C. | 取代反应 | D. | 加成反应 |
20.下列溶液中粒子的物质的量浓度关系正确的是( )
| A. | 0.1mol•L-1NaHC2O4溶液与0.1mol•L-1KOH溶液等体积混合,所得溶液中:c(Na+)>c(K+)>c(C2O42-)>c(OH-)>c(HC2O4-) | |
| B. | 20mL 0.1 mol•L-1 NH4Cl溶液与10mL 0.1mol•L-1NaOH溶液混合后溶液呈碱性,所得溶液中:c(Cl-)>c(NH4+)>c(Na+)>c(OH-)>c(H+) | |
| C. | 常温下,pH=2的HF溶液与pH=12的氢氧化钠溶液等体积混合,所得溶液中:c(Na+)+c(OH-)>c(H+)+c(F-) | |
| D. | 0.1mol•L-1 NH3•H2O溶液与0.1mol•L-1HNO3等体积混合,所得溶液中:c(H+)>c(OH-)+c(NH3•H2O) |
17.下列有关说法正确的是( )
| A. | 白铁(镀锌铁皮)镀层破损后铁仍不易腐蚀 | |
| B. | CH3Cl(g)+Cl2(g)$\stackrel{光照}{→}$CH2Cl2(l)+HCl(g)能自发进行,则该反应的△H>0 | |
| C. | MnS悬浊液中滴加少量CuSO4溶液可生成CuS沉淀,则Ksp(CuS)<Ksp(MnS) | |
| D. | 合成氨生产中将NH3液化分离,一定能加快正反应速率,提高H2的转化率 |
18.下列说法正确的是( )
| A. | 碱金属的单质中,锂的还原性最强 | |
| B. | 第IA族元素比第IIA族元素的金属性强 | |
| C. | 同周期中,原子半径随原子序数的增大而减小(稀有气体除外) | |
| D. | 随着核电荷数的递增,第三周期元素的氧化物对应的水化物的酸性逐渐增强 |
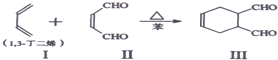
 等.①遇FeCl3溶液显紫色; ②在浓硫酸催化作用下能发生消去反应.
等.①遇FeCl3溶液显紫色; ②在浓硫酸催化作用下能发生消去反应.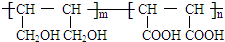 .
.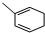 能与CH2=CHCOOH发生类似反应①的反应,生成化合物Ⅷ,写出Ⅷ的一种结构简式为
能与CH2=CHCOOH发生类似反应①的反应,生成化合物Ⅷ,写出Ⅷ的一种结构简式为 .
.