题目内容
17.物质A有如下合成路线:
(1)A的分子式为C9H8O2,含有的官能团为碳碳双键、醛基、酚羟基(写名称).
(2)A→C的化学方程式为
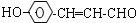 +2Ag(NH3)2OH$\stackrel{△}{→}$
+2Ag(NH3)2OH$\stackrel{△}{→}$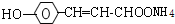 +2Ag↓+3NH3+H2O,反应类型为氧化反应
+2Ag↓+3NH3+H2O,反应类型为氧化反应(3)B的同分异构H、G能与浓溴水反应,且结构中均含有一个-CH3,1mol F消耗3molBr2,1mol G消耗2mol Br2,H的结构简式
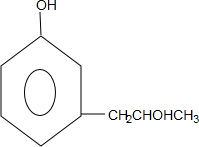 ,G的结构简式
,G的结构简式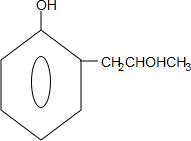 .
.(4)将2滴溴水滴加到大量F中,没有明显现象,若向该溶液中滴加NaOH溶液,有白色沉淀析出.解释上述实验现象原因生成物
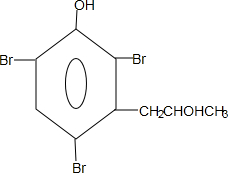 能够溶于有机物,不溶于水,所以在NaOH溶液中出现白色沉淀
能够溶于有机物,不溶于水,所以在NaOH溶液中出现白色沉淀(5)已知在一定条件下R1CH=CHR2→R1CHO+R2CHO,A在一定条件下氧化生成羧酸X、Y,X的分子式为C7H6O2,它是芳香族化合物,Y是一种还原性的二元羧酸.写出两类含有醛基X的同分异构体
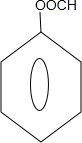 ,
,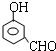 或
或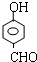 或
或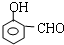 .
.
分析 A能发生显色反应说明A中含有酚羟基,A能和银氨溶液反应说明含有醛基;A发生银镜反应生成C、C酸化生成D、D发生加成反应生成E,A中含有醛基和酚羟基,则A中至少含有2个O原子,则从A到E碳原子个数不变、O原子个数增多1个、H原子个数增多2个,则A的分子式为C9H8O2,A的不饱和度=$\frac{9×2+2-8}{2}$=6,苯环的不饱和度为4、醛基的不饱和度为1,则A中还含有一个碳碳双键;
A和2mol氢气发生加成反应生成B,B中不含甲基,则A的结构简式为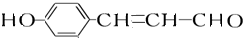 ,1molA与2mol氢气加成生成的B结构简式为
,1molA与2mol氢气加成生成的B结构简式为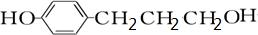 ,A中醛基被氧化生成羧酸铵,C结构简式为
,A中醛基被氧化生成羧酸铵,C结构简式为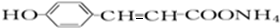 ,C酸化得到D,D结构简式为
,C酸化得到D,D结构简式为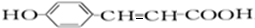 ,D和1mol氢气发生加成反应生成E,E结构简式为
,D和1mol氢气发生加成反应生成E,E结构简式为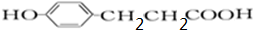 ,E和溴发生取代反应生成F,F仅有一种结构,结合F分子式知F结构简式为
,E和溴发生取代反应生成F,F仅有一种结构,结合F分子式知F结构简式为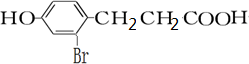 ,据此分析解答.
,据此分析解答.
解答 解:A能发生显色反应说明A中含有酚羟基,A能和银氨溶液反应说明含有醛基;A发生银镜反应生成C、C酸化生成D、D发生加成反应生成E,A中含有醛基和酚羟基,则A中至少含有2个O原子,则从A到E碳原子个数不变、O原子个数增多1个、H原子个数增多2个,则A的分子式为C9H8O2,A的不饱和度=$\frac{9×2+2-8}{2}$=6,苯环的不饱和度为4、醛基的不饱和度为1,则A中还含有一个碳碳双键;
A和2mol氢气发生加成反应生成B,B中不含甲基,则A的结构简式为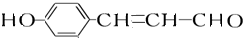 ,1molA与2mol氢气加成生成的B结构简式为
,1molA与2mol氢气加成生成的B结构简式为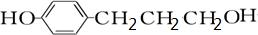 ,A中醛基被氧化生成羧酸铵,C结构简式为
,A中醛基被氧化生成羧酸铵,C结构简式为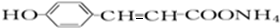 ,C酸化得到D,D结构简式为
,C酸化得到D,D结构简式为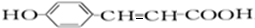 ,D和1mol氢气发生加成反应生成E,E结构简式为
,D和1mol氢气发生加成反应生成E,E结构简式为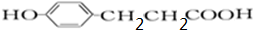 ,E和溴发生取代反应生成F,F仅有一种结构,结合F分子式知F结构简式为
,E和溴发生取代反应生成F,F仅有一种结构,结合F分子式知F结构简式为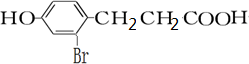 ,
,
(1)A能发生显色反应说明A中含有酚羟基,A能和银氨溶液反应说明含有醛基;A发生银镜反应生成C、C酸化生成D、D发生加成反应生成E,A中含有醛基和酚羟基,则A中至少含有2个O原子,则从A到E碳原子个数不变、O原子个数增多1个、H原子个数增多2个,则A的分子式为C9H8O2,A的不饱和度=$\frac{9×2+2-8}{2}$=6,苯环的不饱和度为4、醛基的不饱和度为1,则A中还含有一个碳碳双键;A和2mol氢气发生加成反应生成B,B中不含甲基,则A的结构简式为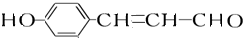 ,分子式为C9H8O2,含有的官能团有碳碳双键、醛基、酚羟基,故答案为:C9H8O2;碳碳双键、醛基、酚羟基;
,分子式为C9H8O2,含有的官能团有碳碳双键、醛基、酚羟基,故答案为:C9H8O2;碳碳双键、醛基、酚羟基;
(2)A中醛基被氧化生成羧酸铵,C结构简式为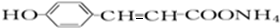 ,化学方程式为
,化学方程式为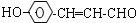 +2Ag(NH3)2OH$\stackrel{△}{→}$
+2Ag(NH3)2OH$\stackrel{△}{→}$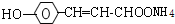 +2Ag↓+3NH3+H2O,
+2Ag↓+3NH3+H2O,
故答案为: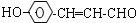 +2Ag(NH3)2OH$\stackrel{△}{→}$
+2Ag(NH3)2OH$\stackrel{△}{→}$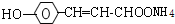 +2Ag↓+3NH3+H2O;氧化反应;
+2Ag↓+3NH3+H2O;氧化反应;
(3)1molA与2mol氢气加成生成的B结构简式为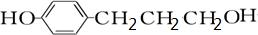 ,其与浓溴水在酚羟基的邻对位上发生取代反应,结构中均含有一个-CH3,1mol H消耗3molBr2,说明酚羟基的邻对位上都能够发生取代反应,取代基在间位上,H可以是
,其与浓溴水在酚羟基的邻对位上发生取代反应,结构中均含有一个-CH3,1mol H消耗3molBr2,说明酚羟基的邻对位上都能够发生取代反应,取代基在间位上,H可以是 ;1mol G消耗2mol Br2,说明另一取代基在邻对位上,可以是
;1mol G消耗2mol Br2,说明另一取代基在邻对位上,可以是 ,
,
故答案为: ;
; ;
;
(4)1mol F消耗3molBr2,说明酚羟基的邻对位上都能够发生取代反应,取代基在间位上,F可以是 ,其与浓溴水发生取代反应,生成的
,其与浓溴水发生取代反应,生成的 ,生成物能够溶于有机物,不溶于水,所以在NaOH溶液中出现白色沉淀,
,生成物能够溶于有机物,不溶于水,所以在NaOH溶液中出现白色沉淀,
故答案为:生成物 能够溶于有机物,不溶于水,所以在NaOH溶液中出现白色沉淀;
能够溶于有机物,不溶于水,所以在NaOH溶液中出现白色沉淀;
(5)X的分子式为C7H6O2,其不饱和度为$\frac{7×2+2-6}{2}$=5,苯环有4个不饱和度,只有7个C原子,所以除苯环外还有1个醛基,两类含有醛基X的同分异构体为 ;
; 或
或 或
或 ,故答案为:
,故答案为: ;
; 或
或 或
或 .
.
点评 本题考查有机物推断,侧重考查学生分析推断能力,为高考高频点,正确推断A的结构简式是解本题关键,再结合反应物的量、反应条件、某些物质的分子式进行推断.

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案| A. | 10g O2和10gH2 | B. | 5.6LN2(标准状况)和11gCO2 | ||
| C. | 9gH2O和0.5molBr2 | D. | 224mL H2(标准状况)和0.1molN2 |
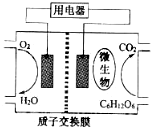 科学家近年来研制出一种新型细菌燃料电池.以葡萄糖为燃料的微生物燃料电池结构示意图如图所示.关于该电池的叙述正确的是( )
科学家近年来研制出一种新型细菌燃料电池.以葡萄糖为燃料的微生物燃料电池结构示意图如图所示.关于该电池的叙述正确的是( )| A. | 该电池的负极反应为O2+2H2O+4e-=4OH- | |
| B. | 电池的负极反应为:C6H12O6+6H2O=6CO2↑+24H++24e- | |
| C. | 放电过程中,H+从正极区向负极区迁移 | |
| D. | 在电池反应中,每消耗1mol氧气,理论上能生成标准状况下CO2气体22.4L |
| A. | 硅是良好的半导体材料,可以与NaOH 溶液和氢氟酸反应 | |
| B. | 二氧化硅与石灰石反应:SiO2+CaCO3$\frac{\underline{\;高温\;}}{\;}$CaSiO3+CO↑ | |
| C. | 用焦炭还原二氧化硅生产硅:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO2↑ | |
| D. | 工业制造镁粉是将镁蒸气在某气体中冷却,CO2可作为冷却气体. |
| A. | O2:二氧化锰和双氧水 带火星的木条 | |
| B. | Cl2:二氧化锰和浓盐酸 品红溶液 | |
| C. | CO2:大理石和稀硫酸 澄清石灰水 | |
| D. | NH3:NH4Cl固体和NaOH固体 湿润的红色石蕊试纸 |
| A. | 该周期有32种元素 | |
| B. | 该周期的元素,原子序数最大为118 | |
| C. | 该周期的ⅦA族元素是金属元素 | |
| D. | 该周期的ⅢA族元素的氢氧化物具有两性 |
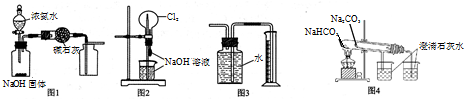
| A. | 图1装置可制取、收集干燥纯净的NH3 | |
| B. | 图2装置可以完成“喷泉”实验 | |
| C. | 图3装置可测量Cu 与浓硝酸反应产生气体的体积 | |
| D. | 图4装置可用比较NaHCO3和Na2CO3的热稳定性 |
| A. | 在测定中和反应的反应热实验中,要读取最高温度 | |
| B. | 中和滴定实验中,洗净后的锥形瓶不需要干燥 | |
| C. | 向CH3COONa溶液中滴入石蕊试液,溶液变蓝 | |
| D. | 向白色ZnS沉淀上滴加CuSO4溶液,沉淀变为黑色,说明Ksp(ZnS)<Ksp(CuS) |