题目内容
2.有关气体制备所用试剂及检验气体所用试剂完全正确的组合是( )| A. | O2:二氧化锰和双氧水 带火星的木条 | |
| B. | Cl2:二氧化锰和浓盐酸 品红溶液 | |
| C. | CO2:大理石和稀硫酸 澄清石灰水 | |
| D. | NH3:NH4Cl固体和NaOH固体 湿润的红色石蕊试纸 |
分析 A.二氧化锰作催化剂,双氧水分解生成氧气,具有助燃性;
B.能够使品红褪色的可以是氯气、二氧化硫,检验氯气通常用湿润的淀粉碘化钾试纸;
C.大理石和稀硫酸反应生成微溶物硫酸钙;
D.实验室制备氨气用氯化铵和消石灰.
解答 解:A.二氧化锰作催化剂,双氧水分解生成氧气,具有助燃性,则带火星的木条复燃可证明氧气,故A正确;
B.二氧化锰和浓盐酸在加热条件下可生成氯气,用湿润的淀粉碘化钾试纸检验,故B错误;
C.大理石和稀硫酸反应生成硫酸钙微溶,附在大理石上使反应难以顺利进行,应用大理石和盐酸反应制取二氧化碳气体,故C错误;
D.实验室制备氨气用氯化铵和消石灰在加热的条件下反应,用NaOH固体在加热的条件下易使试管炸裂,故D错误;
故选:A.
点评 本题考查常见气体的制备和性质的检验,把握反应原理及气体的检验方法为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
12.下列离子方程式的书写正确的是( )
| A. | 稀硫酸与Ba(OH)2溶液反应:SO42-+Ba2+═BaSO4↓ | |
| B. | 向氯化亚铁溶液中通入Cl2:Fe2++Cl2═Fe3++2Cl- | |
| C. | 铁和稀盐酸的反应:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 碳酸镁与稀硫酸的反应:MgCO3+2H+═Mg2++H2O+CO2↑ |
13.蛋白质发生的下列反应中,可逆的是( )
| A. | 盐析 | B. | 变性 | C. | 煮熟 | D. | 加入硫酸钠 |
7.设NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 1 mol NaHSO4晶体中离子总数为3NA | |
| B. | 2.24L14CH4分子中所含中子数为0.8NA | |
| C. | 0.1L 3 mol•L-1的NH4NO3溶液中含有的NH4+数目为0.3 NA | |
| D. | 标况下,将FeSO4溶液置于空气中,被氧化的Fe2+为0.2 NA,吸收O2为1.12 L |
14.为了延长食品的保质期,防止食品受潮及富脂食品氧化变质,在包装袋中可装入的物质是( )
| A. | 无水硫酸铜、蔗糖 | B. | 硅胶、硫酸亚铁 | C. | 食盐、硫酸亚铁 | D. | 生石灰、食盐 |
11. 某无色溶液,可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现各取两份100mL溶液进行如下实验:
某无色溶液,可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现各取两份100mL溶液进行如下实验:
①第一份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为9.32g.
②第二份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图.
已知:2Al3++2CO32-+3H2O=2Al(OH)3↓+3CO2↑
(1)由此推断,原溶液一定含有的阳离子种类及其浓度,将结果填入下表(可不填满).
(2)无法确定的离子是NO3-,如何通过进一步实验确证未确定的离子是否存在?用小试管取少量溶液,加入少量浓硫酸,再向试管中加入铜屑并加热,产生的气体在空气中变成红棕色证明含有硝酸根离子..
 某无色溶液,可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现各取两份100mL溶液进行如下实验:
某无色溶液,可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现各取两份100mL溶液进行如下实验:①第一份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为9.32g.
②第二份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图.
已知:2Al3++2CO32-+3H2O=2Al(OH)3↓+3CO2↑
(1)由此推断,原溶液一定含有的阳离子种类及其浓度,将结果填入下表(可不填满).
| 一定含有的阳离子种类 | ||||||
| 物质的量浓度(mol/L) |
1.在前一种分散系中慢慢地滴入后一种溶液所观察到的现象不是先沉淀后变澄清的是( )
| A. | 氢氧化铁胶体滴加盐酸 | B. | 四羟基合铝酸钠溶液中加盐酸 | ||
| C. | 氯化铝溶液中滴加氢氧化钠溶液 | D. | 氯化铝溶液中滴加氨水 |


 .
. 结构且能水解的所有同分异构体的结构简式:
结构且能水解的所有同分异构体的结构简式: .
.
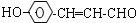 +2Ag(NH3)2OH$\stackrel{△}{→}$
+2Ag(NH3)2OH$\stackrel{△}{→}$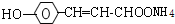 +2Ag↓+3NH3+H2O,反应类型为氧化反应
+2Ag↓+3NH3+H2O,反应类型为氧化反应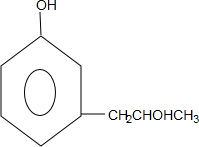 ,G的结构简式
,G的结构简式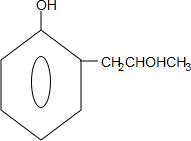 .
.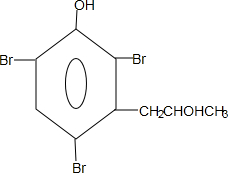 能够溶于有机物,不溶于水,所以在NaOH溶液中出现白色沉淀
能够溶于有机物,不溶于水,所以在NaOH溶液中出现白色沉淀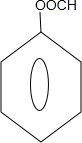 ,
,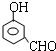 或
或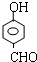 或
或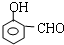 .
.