题目内容
19.写出1---18号元素中符合下列条件的原子(离子)结构示意图:①原子核外M电子层上有2个电子的原子;
②得到2个电子后,其电子层结构与Ne相同的离子;
③微粒带有一个单位的正电荷,核电荷数为11;
④微粒核外有18个电子,当失去1个电子时呈电中性;
⑤微粒不带电,其质数量为1
依次写出各微粒的结构示意图:
 、
、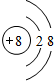 、
、 、
、 、
、 .
.
分析 ①原子核外M电子层上有2个电子,则处于ⅡA,①为Mg原子;②原子得到2个电子后,其电子层结构与Ne相同,②的质子数为10-2=8,②为氧原子;③离子带有一个单位的正电荷,核电荷数为11,则③离子为Na+;D离子核外有18个电子,当失去1个电子时呈电中性,质子数为18-1=17,D离子为Cl-;⑤微粒不带电,其质量数为1,则⑤为H原子,据此解答.
解答 解①原子核外M电子层上有2个电子,则处于ⅡA,①为Mg原子;②原子得到2个电子后,其电子层结构与Ne相同,②的质子数为10-2=8,②为氧原子;③离子带有一个单位的正电荷,核电荷数为11,则③离子为Na+;D离子核外有18个电子,当失去1个电子时呈电中性,质子数为18-1=17,D离子为Cl-;⑤微粒不带电,其质量数为1,则⑤为H原子,结构示意图: ;
;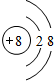 ;
; ;
; ;
; ,
,
故答案为: ;
;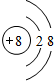 ;
; ;
; ;
; .
.
点评 本题考查物质推断、常用化学用语,侧重对基础知识的巩固,难度不大.

练习册系列答案
 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案
相关题目
7.下列过程中,共价键被破坏的是( )
| A. | 溴挥发 | B. | 氯气被木炭吸附 | C. | 食盐溶于水 | D. | 硫酸溶于水 |
14.H、C、N、O、都属于自然界中常见非金属元素.
(1)O、C、N三种元素的第一电离能由小到大顺序是C O N;NH4+中氮原子轨道的杂化类型为sp3杂化.
(2)CO、N2的结构可表示为:C≡O、N≡N两者的键能数据:(单位kJ/mol)
结合数据说明CO比N2活泼的原因CO的第一个π键的键能为273kJ/mol,N2中的第一个π键的键能为523.3kJ/mol,所以CO的第一个键比N2更容易断裂.
(3)乙二胺(H2N-CH2-CH2-NH2)和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是乙二胺分子间可以形成氢键,三甲胺分子间不能形成氢键.
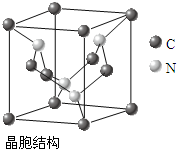
(4)C、N元素形成的新材料具有如右图所示结构,该晶体硬度将超过目前世界上最硬的金刚石,成为首屈一指的超硬新材料.该物质的化学式为:C3N4.
(1)O、C、N三种元素的第一电离能由小到大顺序是C O N;NH4+中氮原子轨道的杂化类型为sp3杂化.
(2)CO、N2的结构可表示为:C≡O、N≡N两者的键能数据:(单位kJ/mol)
| A-B | A=B | A≡B | |
| CO | 357.7 | 798.9 | 1071.9 |
| N2 | 154.8 | 418.4 | 941.7 |
(3)乙二胺(H2N-CH2-CH2-NH2)和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是乙二胺分子间可以形成氢键,三甲胺分子间不能形成氢键.
(4)C、N元素形成的新材料具有如右图所示结构,该晶体硬度将超过目前世界上最硬的金刚石,成为首屈一指的超硬新材料.该物质的化学式为:C3N4.

4.化学与社会、生产、生活紧切相关.下列说法正确的是( )
| A. | 棉花和木材的主要成分都是纤维素,蚕丝和人造丝的主要成分都是蛋白质 | |
| B. | 石油干馏可得到石油气、汽油、煤油、柴油等 | |
| C. | 变质的油脂有特殊难闻气味,是因为油脂发生了氧化反应 | |
| D. | 制作快餐盒的聚苯乙烯塑料是易降解塑料 |
11.今有五种有机物:
①CH2OH(CHOH)4CHO
②CH3(CH2)3OH
③CH2═CH-CH2OH
④CH2═CH-COOCH3
⑤CH2═CH-COOH.
其中既能发生加成反应、加聚反应、酯化反应,又能发生氧化反应的是( )
①CH2OH(CHOH)4CHO
②CH3(CH2)3OH
③CH2═CH-CH2OH
④CH2═CH-COOCH3
⑤CH2═CH-COOH.
其中既能发生加成反应、加聚反应、酯化反应,又能发生氧化反应的是( )
| A. | ③⑤ | B. | ①②⑤ | C. | ②④ | D. | ③④ |
9.下列电子式正确的是( )
| A. | 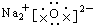 | B. | 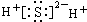 | ||
| C. | 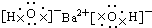 | D. |  |
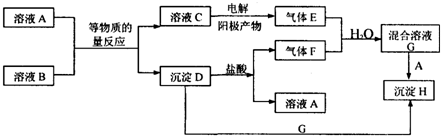
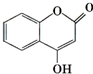 可用来制备抗凝血药,通过下列路线合成:
可用来制备抗凝血药,通过下列路线合成: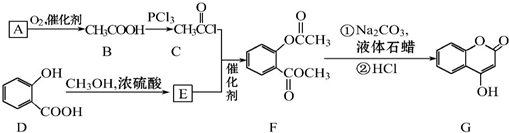
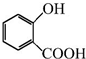 +CH3OH$?_{△}^{浓硫酸}$
+CH3OH$?_{△}^{浓硫酸}$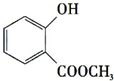 +H2O.
+H2O. +3NaOH$\stackrel{△}{→}$
+3NaOH$\stackrel{△}{→}$ +CH3COONa+CH3OH+H2O.
+CH3COONa+CH3OH+H2O.