题目内容
11.羧基化反应(Carbonylation)指在有机化合物分子内引入羧基或其它基团而成为含氧化合物的一类反应.自1938年首例烯烃羧基化反应发现以后,这类反应一直是有机合成和催化领域的研究特点之一.羧基化反应是制备酸或不饱和酯的有效途径,如:烯烃类的羧基化:乙烯、CO和水蒸气在羧基镍存在下于250~320℃、(1.013~3.039)×103帕条件下反应得到丙酸;炔烃类的羧基化反应:请回答下列问题:

(1)从有机化学角度分析,乙烯、CO和水蒸气合成丙酸的反应属于还原(填“氧化”或“还原”)反应.
(2)化合物Ⅱ的分子式为C10H10O2,化合物Ⅱ在NaOH溶液中完全水解的化学方程式为
 .
.(3)化合物Ⅲ的结构式为
 ,化合物Ⅳ通过消去反应生成化合物Ⅰ的化学方程式为
,化合物Ⅳ通过消去反应生成化合物Ⅰ的化学方程式为 .
.(4)化合物Ⅴ是化合物Ⅱ的同分异构体,其苯环上有两个取代基且能发生银镜反应,Ⅴ的核磁共振氢谱除苯环峰外还有两组峰,峰面积之比为1:2,Ⅴ的结构简式为
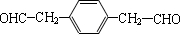 (写一种即可).
(写一种即可).(5)聚合物
 单体的结构简式为
单体的结构简式为 ;利用题中所给信息,自选合适的原料通过一步反应合成该单体,写出其化学方程式
;利用题中所给信息,自选合适的原料通过一步反应合成该单体,写出其化学方程式 .
.
分析 (1)乙烯、CO和水蒸气合成丙酸,可看作乙烯的加成反应,也为还原反应;
(2)化合物Ⅱ含有酯基,可水解;
(3)化合物Ⅲ可发生加成反应,应含有碳碳双键,化合物Ⅳ含有碳碳双键和溴原子,消去反应生成碳碳三键;
(4)化合物Ⅴ是化合物Ⅱ的同分异构体,其苯环上有两个取代基且能发生银镜反应,说明含有醛基,Ⅴ的核磁共振氢谱除苯环峰外还有两组峰,峰面积之比为1:2,说明结构对称,且含有-CH2-、-CHO;
(5)聚合物 单体为
单体为 ,可由丙炔、CO和甲醇合成.
,可由丙炔、CO和甲醇合成.
解答 解:(1)乙烯、CO和水蒸气合成丙酸,可看作乙烯的加成反应,也为还原反应,故答案为:还原;
(2)化合物Ⅱ的分子式为C10H10O2,化合物Ⅱ含有酯基,可水解,方程式为 ,
,
故答案为:C10H10O2; ;
;
(3)化合物Ⅲ可发生加成反应,应含有碳碳双键,由加成产物可知结构简式为 ,化合物Ⅳ含有碳碳双键和溴原子,消去反应生成碳碳三键,方程式为
,化合物Ⅳ含有碳碳双键和溴原子,消去反应生成碳碳三键,方程式为 ,
,
故答案为: ;
; ;
;
(4)化合物Ⅴ是化合物Ⅱ的同分异构体,其苯环上有两个取代基且能发生银镜反应,说明含有醛基,Ⅴ的核磁共振氢谱除苯环峰外还有两组峰,峰面积之比为1:2,说明结构对称,且含有-CH2-、-CHO,对应结构为 ,故答案为:
,故答案为: ;
;
(5)聚合物 单体为
单体为 ,可由丙炔、CO和甲醇合成,方程式为
,可由丙炔、CO和甲醇合成,方程式为 ,
,
故答案为: ;
; .
.
点评 本题考查有机物的合成,为高考常见题型,侧重于学生的分析能力的考查,答题时注意把握官能团的性质以及题给信息,难度中等.

练习册系列答案
相关题目
6.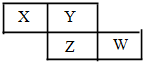 X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如下图所示.若Y原子的最外层电子是 k层电子数的3倍,下列说法不正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如下图所示.若Y原子的最外层电子是 k层电子数的3倍,下列说法不正确的是( )
 X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如下图所示.若Y原子的最外层电子是 k层电子数的3倍,下列说法不正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如下图所示.若Y原子的最外层电子是 k层电子数的3倍,下列说法不正确的是( )| A. | 氢化物的熔、沸点:H2Y>H2Z | |
| B. | 元素X、Z的最高价氧化物对应的水化物都是强酸 | |
| C. | W元素的阴离子与Ar原子具有相同的电子层结构 | |
| D. | X与Y形成的化合物都易溶于水 |
7.在城市中地下常埋有纵横交错的管道和输电线路,有些地面上还铺有地铁或城铁的铁轨,当有电流泄露入潮湿的土壤中,并与金属管道或铁轨形成回路时.就会引起后者的腐蚀.原理简化如图所示.则下列有关说法不正确的是( )
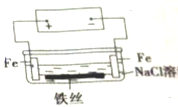

| A. | 原理图可理解为两个串联电解装置 | |
| B. | 溶液中铁丝被腐蚀时,左侧有无色气体产生,附近产生少量白色沉淀,随后变为灰绿色 | |
| C. | 溶液中铁丝左端电极反应式为:Fe-2e-═Fe2+ | |
| D. | 地下管线被腐蚀,不易发现,维修也不便,故应将埋在地下的金属管道表面涂绝缘膜(或油漆等) |
6. 醇是重要的有机化工原料.一定条件下,甲醇可同时发生下面两个反应:
醇是重要的有机化工原料.一定条件下,甲醇可同时发生下面两个反应:
i.2CH3OH(g)?CH3OCH3(g)+H2O(g)
ii.2CH3OH(g)?C2H4(g)+2H2O(g)
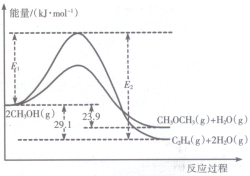
I.上述反应过程中能量变化如图所示:
(1)在某密闭容器中,充人一定量CH3OH(g)发生上述两个反应,反应i(填“i”或“ii”)的速率较大,其原因为该反应的活化能较小.若在容器中加入催化剂,使ii的反应速率增大,则E1和E2-E1的变化是:E1减小;E2-E1不变(填“增大”、“减小”或“不变”).
(2)已知:CH3CH2OH(g)=CH3OCH3(g)△H=+50.7kJ.mol-1.则乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g)的△H=-45.5kJ•mol-1.
Ⅱ,某研究小组通过控制反应条件,在三个容积均为2L的密闭容器中只发生反应i,起始反应温度均为T℃,起始投料如下表所示:
(3)比较平衡时容器1中c1(H2O)和容器2中c2(H2O)的大小:c1(H2O)<c2(H2O)(填“>”、“<”或“=”);三个容器中反应的化学平衡常数分别记为K1、K2和K3,三者的大小关系为K1=K2>K3.
(4)若容器l中平衡时CH3OH(g) 的转化率为80%,则该温度下反应i的平衡常数K=4.
 醇是重要的有机化工原料.一定条件下,甲醇可同时发生下面两个反应:
醇是重要的有机化工原料.一定条件下,甲醇可同时发生下面两个反应:i.2CH3OH(g)?CH3OCH3(g)+H2O(g)
ii.2CH3OH(g)?C2H4(g)+2H2O(g)
I.上述反应过程中能量变化如图所示:
(1)在某密闭容器中,充人一定量CH3OH(g)发生上述两个反应,反应i(填“i”或“ii”)的速率较大,其原因为该反应的活化能较小.若在容器中加入催化剂,使ii的反应速率增大,则E1和E2-E1的变化是:E1减小;E2-E1不变(填“增大”、“减小”或“不变”).
(2)已知:CH3CH2OH(g)=CH3OCH3(g)△H=+50.7kJ.mol-1.则乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g)的△H=-45.5kJ•mol-1.
Ⅱ,某研究小组通过控制反应条件,在三个容积均为2L的密闭容器中只发生反应i,起始反应温度均为T℃,起始投料如下表所示:
| 起始投料/mol 编号 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
| 恒温容器1 | 2 | 0 | 0 |
| 恒温容器2 | 0 | 2 | 2 |
| 绝热容器3 | 2 | 0 | 0 |
(4)若容器l中平衡时CH3OH(g) 的转化率为80%,则该温度下反应i的平衡常数K=4.
16.对硫代硫酸钠中硫元素价态有三种意见:(1)由于硫与亚硫酸钠加热可生成硫代硫酸钠,所以Na2S2O3中硫元素价态分别为0价,+4价;(2)硫平均价态为+2价;(3)硫代硫酸钠是硫酸钠中的一个氧原子换成硫原子,硫的价态分别为-2、+6价.下列对硫代硫酸钠和反应Na2S2O3+H2SO4=S↓+SO2↑+Na2SO4+H2O的分析正确的是( )
| A. | 三种意见都支持上述反应为氧化还原反应,且电子转移数相同 | |
| B. | 通过闻生成气体气味可判断反应快慢 | |
| C. | 用稀硫酸可鉴别硫代硫酸钠、亚硫酸钠溶液 | |
| D. | 生成的气体可漂白酸性高锰酸钾溶液 |
3.在3个2L的密闭容器中,在相同的温度下、使用相同的催化剂分别进行反应:3H2(g)+N2(g)$?_{催化剂}^{高温、高压}$2NH3(g).按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:下列说法不正确的是( )
| 容器 | 甲 | 乙 | 丙 |
| 反应物的投入量 | 3molH2、2molN2 | 6molH2、4molN2 | 2molNH3 |
| 达到平衡的时间/min | 5 | 8 | |
| 平衡时N2的浓度/mol•L-1 | c1 | 1.5 | |
| NH3的体积分数 | φ1 | φ2 | |
| 混合气体的密度/g•L-1 | ρ1 | ρ2 |
| A. | 容器乙中反应从开始到达平衡的反应速率为v(H2)=0.3mol•L-1•min-1 | |
| B. | 在该温度下甲容器中反应的平衡常数K=$\frac{(2-2{c}_{1})^{2}}{{c}_{1}•(3{c}_{1}-1.5)}$ | |
| C. | 2c1<1.5 | |
| D. | 2ρ1=ρ2 |
1.下列各组中属于同位素关系的是( )
| A. | H2与D2 | B. | T2O与H2O | ||
| C. | ${\;}_{19}^{40}$K与${\;}_{19}^{39}$K | D. | 金刚石与石墨 |