题目内容
11.下列变化中必须加入适当的氧化剂才能实现的是( )| A. | MnO2→Mn2+ | B. | PCl3→PCl5 | C. | HCl→H2 | D. | H2O2→O2 |
分析 氧化剂具有氧化性,在反应中得到电子,必须加入氧化剂才能实现的反应,选项中涉及物质被氧化,所含元素的化合价升高,以此解答.
解答 解:A.Mn元素化合价降低,被还原,应该加入还原剂,故A错误;
B.P元素化合价升高,被氧化,应加入氧化剂才能实现,故B正确;
C.H元素化合价降低,被还原,应该加入还原剂,故C错误;
D.O元素化合价升高,被氧化,但可通过自身发生氧化还原反应实现,故D错误.
故选B.
点评 本题考查氧化还原反应,侧重于学生的分析能力的考查,为高考常见题型,注意把握常见反应的特点以及物质的性质,学习中注意相关基础知识的积累,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.不能用胶体知识解释的是( )
| A. | 静电除尘 | |
| B. | 一支钢笔用不同牌子的两种墨水,易堵塞 | |
| C. | 氯化铁溶液加入碳酸钠溶液出现红褐色沉淀 | |
| D. | 河水和海水交界处形成三角洲 |
19.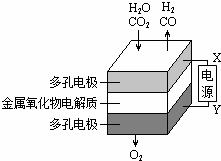 在固态金属氧化物电解池中,高温共电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温共电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
 在固态金属氧化物电解池中,高温共电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温共电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )| A. | X是电源的负极 | |
| B. | 阴极的反应式是:H2O+2eˉ=H2+O2ˉ | |
| C. | 总反应可表示为:H2O+CO2=H2+CO+O2 | |
| D. | 阴、阳两极生成的气体的物质的量之比是2:1 |
16.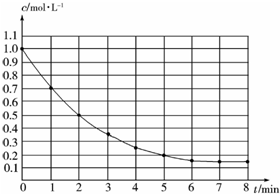 如图表示反应X(g)?4Y(g)+Z(g)△H<0,在某温度时X的浓度随时间变化的曲线,下列有关该反应的描述正确的是( )
如图表示反应X(g)?4Y(g)+Z(g)△H<0,在某温度时X的浓度随时间变化的曲线,下列有关该反应的描述正确的是( )
 如图表示反应X(g)?4Y(g)+Z(g)△H<0,在某温度时X的浓度随时间变化的曲线,下列有关该反应的描述正确的是( )
如图表示反应X(g)?4Y(g)+Z(g)△H<0,在某温度时X的浓度随时间变化的曲线,下列有关该反应的描述正确的是( )| A. | X的平衡转化率为85% | |
| B. | 第6 min 后,反应就终止了 | |
| C. | 若升高温度,X的平衡转化率将大于85% | |
| D. | 若降低温度,v正减小,v逆增大 |
1.已知,石墨在一定条件下可转化为金刚石,已知12g石墨完全转化为金刚石时,要吸收1.91kJ的热量,据此判断,下列说法中正确的是( )
| A. | 由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的低 | |
| B. | 由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的高 | |
| C. | 由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的低 | |
| D. | 由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的高 |
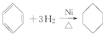
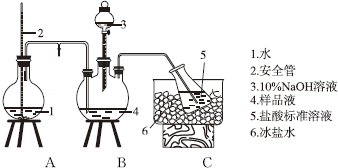
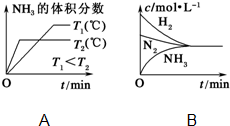 已知工业上合成氨反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,回答以下问题:
已知工业上合成氨反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,回答以下问题: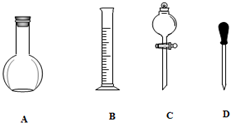 实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.
实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.